Тема: Белки - природные биополимеры
“Меняя каждый миг свой образ прихотливый,
капризна, как дитя, и призрачна, как дым,
кипит повсюду жизнь в тревоге суетливой,
великое смешав с ничтожным и смешным…”
С.Я. Надсон
| Методическая информация |
||||||||||||||||||||||||||||||
| Тип занятия | Интегрированный (биология + химия) проблемно-исследовательский мультимедиа урок |
|||||||||||||||||||||||||||||
| Формировать у обучающихся представление о свойствах и функциях белков в клетке и организме |
||||||||||||||||||||||||||||||
| Обучающие: дать понятие о белках - природных биополимерах, их многообразных функциях, химических свойствах белков; формировать знания об уникальных особенностях строения белков; углубить знания о взаимосвязи строения и функции веществ на примере белков; учить обучающихся, использованию знаний смежных предметов для получения более полной картины мира. Развивающие: развитие познавательного интереса, установление межпредметных связей; совершенствовать умения анализировать, сравнивать, устанавливать взаимосвязь между строением и свойствами. Воспитательные: показать материальное единство органического мира; формирование научного мировоззрения; |
||||||||||||||||||||||||||||||
| Метод проблемного изложения, частично-поисковый, эвристический, исследовательский |
||||||||||||||||||||||||||||||
| Функция преподавателя: | Управляющий поисковой работой обучающихся, консультант |
|||||||||||||||||||||||||||||
| Знания, умения, навыки и компетенции, которые обучающиеся актуализируют, приобретут, закрепят в ходе занятия: | Формируются такие мыслительные операции, как: сравнение свойств белка, классификация структур белковой молекулы, сравнительный анализ функций белка. Основные понятия: Аминокислоты, пептидная связь, полипептид, структура белка, функции белка, свойства белка, денатурация. Основные навыки: Работа с химическим оборудованием, работа по выявлению активности каталазы |
|||||||||||||||||||||||||||||
| Необходимое оборудование и материалы: | Компьютер, презентация по теме урока. Эксперимент: пробирки, штативы, спиртовка, держатель. Реактивы и материалы: р-р Белка куриного яйца, азотная кислота, р-р сульфата меди(II), щелочь, раствор 3% перекиси водорода, сырой и вареный картофель или мясо. |
|||||||||||||||||||||||||||||
| Ведущий тип деятельности: | Продуктивный, творческий, проблемный |
|||||||||||||||||||||||||||||
| Технологическая карта занятия |
||||||||||||||||||||||||||||||
| Мотивация: | Как изучение этой темы может вам помочь в вашей будущей профессии? |
|||||||||||||||||||||||||||||
| Ход занятия: |
||||||||||||||||||||||||||||||
| Организационный момент | “Белки, жиры и углеводы, |
|||||||||||||||||||||||||||||
| Актуализация знаний | А знаете ли Вы: 8. Как появилась жизнь на Земле? Что лежит в основе жизни? Вот сегодня мы об этом и будем вести речь. План занятия: Определение. Функции белков. Состав и строение белков. Структура белков. Химические свойства белков. 6. Превращение белков в организме. |
|||||||||||||||||||||||||||||
| Проблемный вопрос? Как строение белка может быть связано с его свойствами и функциями? Гипотеза: Примеры белков История открытия: Состав белков Определение | Понять, каким образом белки осуществляют перечисленные выше многообразные функции, непросто. Единственный способ приблизиться к решению этой задачи - узнать, из чего построен белок, как расположены структурные элементы, составляющие его молекулу, по отношению друг к другу и в пространстве, как они взаимодействуют друг с другом и веществами внешней среды, т.е. изучить строение и свойства белков. |
|||||||||||||||||||||||||||||
| Раскрыть причинно- следственную зависимость: функции - строение. белки - полимеры, мономеры - аминокислоты |
||||||||||||||||||||||||||||||
| Назовите известные вам белки, укажите их местонахождение? глобулин - вакцина, родопсин - зрительный пурпур, В середине 19 века положено начало изучения белков, но только через 100 лет учёные систематизировали белки, определи их состав, а также сделали вывод, что белки - это главный компонент живых организмов. А.Я. Данилевский - наличие в белке пептидной связи Э.Фишер - синтезировал соединения белка Химический состав белка может быть представлен следующими данными: С -55%, О - 24%, Н - 7,3%, N - 19%, S -2,4%. На долю белков приходится более 50% общей массы органических соединений животной клетки: в мышцах - 80%, в коже - 63%, в печени - 57%, в мозге - 45%, в костях -28% Химические формулы некоторых белков : Пенициллин С16Н18О4N2 Казеин С1864Н3021О576N468 S2 Гемоглобин С3032Н4816 О872N780S8Fе4 - Давайте дадим определение термину БЕЛОК БЕЛКИ - биополимеры нерегулярного строения, мономерами которого являются 20 аминокислот разных типов. В химический состав аминокислот входят: С, О, Н, N, S. Белковые молекулы могут образовывать четыре простраственные структуры и выполняют в клетке и организме целый ряд функций: строительную, каталитическую, регуляторную, двигательную, транспортную |
||||||||||||||||||||||||||||||
| Функции белков | - Белки - основа живого на Земле, входят в состав кожи, мышечной и нервной ткани, волос, сухожилий, стенок сосудов животных и человека; это строительный материал клетки. Роль белков трудно переоценить, т.о. жизнь на нашей планете действительно можно рассматривать как способ существования белковых тел, осуществляющих обменом веществ и энергией с внешней средой. Поскольку белок содержит разнообразные функциональные группы, он не может быть отнесен к какому-нибудь из ранее изученных классов соединений. В нем как в фокусе сочетаются признаки соединений, относящихся к различным классам. Отсюда его многообразие. Это в сочетании с особенностями его структуры и характеризует белок как высшую форму развития вещества. |
|||||||||||||||||||||||||||||
| Структура белка | Составить конспект и ответить в процессе беседы на вопросы: Остатки каких аминокислот входят в состав молекул белка? (см.прил.) За счёт каких функциональных групп аминокислот происходит соединение их друг с другом? Что понимают под «первичной» структурой белка? Что представляет собой «вторичная» структура белка? Какие связи её удерживают? Что такое «третичная» структура? За счет, каких связей она образуется? В чем особенность четвертичной структуры? (В виде линейной последовательности аминокислот)
-Что собой представляет первичная структура белка? Какие связи стабилизируют вторичную структуру? (Пространственная конфигурация белковой молекулы свернутые в виде спирали. В формировании спиральной конфигурации полипептидной цепи играют роль водородные связи между -С=О и -N-H группами.. )
- Что собой представляет третичная структура белка ? (Э то конфигурация в виде закрученной вспираль полипептидной цепи. Она поддерживается взаимодействием разных функциональных групп полипептидной цепи. Так, между атомами серы образуется дисульфидный мостик, между карбоксильной и гидроксильной группами имеется сложноэфирный мостик, а между карбоксильной и аминогруппами может возникнуть солевой мостик. Для этой структуры характерны и водородные связи).
- Что собой представляет четвертичная структура белка? (Некоторые белковые макромолекулы могут соединяться друг с другом и образовывать относительно крупные агрегаты- макромолекулы белка).
Какие химические свойства будут характерны для белков? (Амфотерность связана с наличием в молекуле белка катионообразующих групп - аминогрупп и анионообразующих - карбоксильных группу. Знак заряда молекулы зависит от количества свободных групп. Если преобладают карбоксильные группы, то заряд молекулы - отрицательный (проявляются свойства слабой кислоты), еслиаминогруппы - то положительный (основные свойства)).
|
|||||||||||||||||||||||||||||
| Химические свойства белков | Для белков характерны реакции, в результате которых выпадает осадок. Но в одних случаях полученный осадок при избытке воды растворяется, а в других - происходит необратимое свертывание белков, т.е. денатурация. Происходит изменение вторичной, третичной и четвертичной структур белковой макромолекулы под влиянием внешних факторов: температура, действия химических реагентов, механического воздействия. При денатурации изменяются физические свойства белка, снижается растворимость, теряется биологическая активность К чему может привести денатурация? Нарушение антигенной чувствительности белка; Блокирование ряда иммунологических реакций; Нарушение обмена веществ; Воспаление слизистой оболочки ряда органов пищеварения (гастриты, колит); Камнеобразование (камни имеют белковую основу). Также для белков характерны: Свертывание белков при нагревании Осаждение белков солями тяжелых металлов и спиртом Белки горят с образованием азота, углекислого газа и воды, а также некоторых других веществ. Горение сопровождается характерным запахом жженых перьев. Белки подвергаются гниению (под действием гнилостных бактерий), при этом образуются метан (CH4), сероводород (H2S), аммиак (NH3), вода и другие низкомолекулярные продукты. Амфотерность Строение АК в общем виде: NH2-CH- COOH, где R - углеводородный радикал. СООН - карбоксильная группа / кислотные свойства/. NН2 - аминогруппа / основные свойства/. Процесс восстановления структуры белка называется ренатурацией Превращения белков в организме. Белки пищи → полипептиды → α-аминокислоты → белки организма |
|||||||||||||||||||||||||||||
| Как ведет себя белок по отношению к воде? |
|
|||||||||||||||||||||||||||||
| Гидролиз | Гидролиз белка - разрушение первичной структуры белка под действием кислот, щелочей или ферментов, приводящее к образованию α- аминокислот, из которых он был составлен.
Белки - Альбумозы - Дипептиды - Аминокислоты |
|||||||||||||||||||||||||||||
| Качественные, цветные реакции на белок | Ксантопротеиновая реакция - реакция на ароматические циклы. Белок + HNO3(к) → белый осадок → желтая окраска → оранжевая окраска + NH3 Как с помощью ксантопротеиновой реакции можно отличить натуральные шерстяные нитки от искусственных? |
|||||||||||||||||||||||||||||
| Биуретовая реакция - реакция на пептидные связи. Белок + Cu(OH)2 → фиолетовая окраска раствора Можно ли с помощью химии решить проблему дефицита белковой пищи? Должна медленно появиться розово-фиолетовая или пурпурная окраска. Это реакция на пептидные связи в соединениях. В присутствии разбавленного раствора Си в щелочной среде атомы азота пептидной цепи образуют окрашенный в пурпурный цвет комплекс с ионами меди (II). Биурет (производное мочевины) тоже содержит группу CONH - и поэтому дает эту реакцию. |
||||||||||||||||||||||||||||||
| Функции белка |
|
|||||||||||||||||||||||||||||
| Домашняя работа | Один стакан цельного молока содержит 288 мг кальция. Сколько нужно выпивать в день молока для снабжения вашего организма достаточным количеством этого элемента? Суточная потребность 800 мг Са. (Ответ. Для удовлетворения суточной потребности в кальции взрослый мужчина должен выпивать в день 2,7 стакана молока: 800 мг Са*(1 стакан молока/ 288 Са) = 2,7 стакана молока). В куске белого пшеничного хлеба 0,8 мг железа. Сколько кусков нужно съедать в день для удовлетворения суточной потребности в этом элементе. (Суточная потребность в железе 18 мг). (Ответ. 22,5 кусочка) 18 мг.: 0,8= 22,5 |
|||||||||||||||||||||||||||||
| Закрепление изученного материала Игра «Подними руку, если согласен» | Сейчас вы будете выполнять задание по изученной теме в виде теста. (Во время проверки обучающиеся меняются своими работами и оценивают работу соседа. Варианты правильных ответов на доске. По окончании проверки каждый выставляет оценку соседу) - Какая структура является самой прочной? Почему?
-Как можно с помощью проволоки, бус показать образование вторичной, третичной, четвертичной структур белка . За счет каких связей, взаимодействий это происходит? А теперь с помощью теста проверим, как вы усвоили материал. На ответ «Да» поднимаете руку. 1. В состав белков входят аминокислоты, прочно связанные между собой водородными связями (Нет) 2. Пептидной называют связь между углеродом карбоксильной группы одной аминокислоты и азотом аминогруппы другой аминокислоты. (Да) 3. Белки составляют основную часть органических веществ клетки. (Да) 4.Белок - мономер. (Нет) 5. Продукт гидролиза пептидных связей - вода. (Нет) 6. Продукты гидролиза пептидных связей - аминокислоты. (Да) 7. Белок - макромолекула. (Да) 8. Катализаторы клетки - это белки. (Да) 9. Существуют белки, переносящие кислород и углекислый газ. (Да) 10. Иммунитет не связан с белками. (Нет) |
|||||||||||||||||||||||||||||
| Высказывания о жизни и белках знаменитых людей | «Повсюду, где мы встречаем жизнь, мы находим, что она связана с каким-либо белковым телом». Ф.Энгельс «Анти-Дюринг» Знаменитый путешественник и естествоиспытатель Александр Гумбольдт еще на пороге 19 века давал такое определение жизни: «Жизнь есть способ существования белковых тел, существенным моментом которого является постепенный обмен веществ с окружающей их внешней природой; причем с прекращением этого обмена веществ прекращается и сама жизнь, что приводит к разложению белка». Определение, данное Ф.Энгельсом в работе«Анти-Дюринг», позволяет задуматься над тем, как современная наука представляет процесс жизни. «Жизнь - это переплетение сложнейших химических процессов взаимодействия белков между собой и другими веществами». |
|||||||||||||||||||||||||||||
Приложение № 1
Функции белков.
Каталитическая функция
Белок как фермент: Ферменты - белки, обладающие каталитической активностью, т.е. ускоряющие протекание реакций. Все ферменты катализируют только одну реакцию. Заболевания, вызываемые ферментной недостаточностью.
Пример: неперевариваемость молока (нет фермента лактазы); гиповитаминозы (витаминная недостаточность)
Определение активности ферментов в биологических жидкостях имеет большое значение для диагностики заболевания. Например, по активности ферментов в плазме крови определяют вирусный гепатит.
Ферменты используют как реактивы при диагностике некоторых заболеваний.
Ферменты используют для лечения некоторых болезней. Примеры: панкреатин, фестал, лидаза.
Ферменты используются в промышленности: при приготовлении безалкогольных напитков, сыров, консервов, колбас, копченостей.
Ферменты используются при обработке льна, конопли, для смягчения кожи в кожевенной промышленности, они входят в состав стиральных порошков.
Структурная функция
Белки являются структурным компонентом многих клеток. Например, мономеры актина итубулина — это глобулярные, растворимые белки, но после полимеризации они формируют длинные нити, из которых состоит цитоскелет, позволяющий клетке поддерживать форму.Коллаген и эластин — основные компоненты межклеточного вещества соединительной ткани (например, хряща), а из другого структурного белка кератина состоят волосы, ногти,перья птиц и некоторые раковины.
Защитная функция
Существуют несколько видов защитных функций белков:
Физическая защита. В ней принимает участие коллаген — белок, образующий основу межклеточного вещества соединительных тканей (в том числе костей, хряща, сухожилий и глубоких слоёв кожи (дермы)); кератин, составляющий основу роговых щитков, волос, перьев, рогов и др. производных эпидермиса.
Химическая защита. Связывание токсинов белковыми молекулами может обеспечивать их детоксикацию. Особенно важную роль в детоксикации у человека играютферментыпечени, расщепляющие яды или переводящие их в растворимую форму, что способствует их быстрому выведению из организма.
Иммунная защита. Белки, входящие в состав крови и других биологических жидкостей, участвуют в защитном ответе организма как на повреждение, так и на атакупатогенов
Регуляторная функция
Многие процессы внутри клеток регулируются белковыми молекулами, которые не служат ни источником энергии, ни строительным материалом для клетки. Эти белки регулируюттранскрипцию, трансляцию, а также активность других белков и др.
Регуляторную функцию белки осуществляют либо за счёт ферментативной активности), либо за счёт специфического связывания с другими молекулами, как правило, влияющего на взаимодействие с этими молекулами ферментов.
Сигнальная функция
Сигнальная функция белков — способность белков служить сигнальными веществами, передавая сигналы между клетками, тканями, о́рганами и разными организмами. Часто сигнальную функцию объединяют с регуляторной, так как многие внутриклеточные регуляторные белки тоже осуществляют передачу сигналов.
Сигнальную функцию выполняют белки-гормоны, цитокины, факторы роста и др.
Транспортная функция
Примером транспортных белков можно назвать гемоглобин, который переносит кислород из лёгких к остальным тканям и углекислый газ от тканей к лёгким, а также гомологичные ему белки, найденные во всех царствах живых организмов.
Запасная (резервная) функция белков
К таким белкам относятся так называемые резервные белки, которые запасаются в качестве источника энергии и вещества в семенах растений и яйцеклетках животных; белки третичных оболочек яйца (овальбумины) и основной белок молока (казеин) также выполняют, главным образом, питательную функцию. Ряд других белков используется в организме в качестве источника аминокислот, которые в свою очередь являются предшественниками биологически активных веществ, регулирующих процессыметаболизма.
Рецепторная функция
Белковые рецепторы могут как находиться в цитоплазме, так и встраиваться в клеточную мембрану. Одна часть молекулы рецептора воспринимает сигнал, которым чаще всего служит химическое вещество, а в некоторых случаях — свет, механическое воздействие (например, растяжение) и другие стимулы. При воздействии сигнала на определённый участок молекулы — белок-рецептор — происходят её конформационные изменения. В результате меняется конформация другой части молекулы, осуществляющей передачу сигнала на другие клеточные компоненты.
Моторная (двигательная) функция
Целый класс моторных белков обеспечивает движения организма, например, сокращение мышц, в том числе локомоцию (миозин), перемещение клеток внутри организма (например, амебоидное движение лейкоцитов), движение ресничек и жгутиков, а также активный и направленный внутриклеточный транспорт создайте презентацию
Коды пищевых добавок
| Е103, Е105, Е111, Е121, Е123,Е125,Е126, Е130, Е152. |
|
| 2. Подозрительные | Е104, ЕЕ122, Е141, Е150, Е171, Е173, Е180, Е241, Е477. |
| 3. Опасные | Е102, Е110, Е120, Е124,. Е127. |
| 4.Канцерогенные | Е131,Е210-Е217,Е240, Е330. |
| 5. Вызывающие расстройства кишечника | |
| 6. Вредные для кожи | |
| 7. Вызывающие нарушение давления | |
| 8. Провоцирующие появление сыпи | |
| 9. Повышающие уровень холестерина | |
| 10. Вызывающие расстройство желудка | Е338 Е341, Е407, Е450, Е461 - Е466 |
Практическая работа
Тема: «Химические свойства белков. Качественные (цветные) реакции на белки».
Цель : Изучить химические свойства белков. Познакомиться с качественными реакциями на белки. Активность фермента каталазы в живых и мертвых тканях..
«Денатурация белков»
Порядок выполнения.
Приготовьте раствор белка.
В пробирку налейте 4-5 мл раствора белка и нагрейте до кипения.
Отметьте изменения.
Охладите содержимое пробирки и разбавьте водой.

«Ксантопротеиновая реакция»
Порядок выполнения.
2. В пробирку прилейте 1 мл уксусной кислоты.
3. Содержимое пробирки нагрейте.
4. Охладите смесь и добавьте аммиак до щелочной среды.
5. Отметьте изменения.
« Биуретовая реакция »
Порядок выполнения.
1. В пробирку налейте 2-3 мл раствора белка.
2. Добавьте 2-3 мл раствора гидроксида натрия и 1-2 мл раствора медного купороса..
3. Отметьте изменения.
Качественные (цветные)
реакции на белки. Опыты №2 и №3
Ксантопротеиновая реакция
Белок + HNO3конц > ярко?желтое окрашивание
(обнаружение бензольных ядер)
Биуретовая реакция
Белок + NaOH+CuSO4 > красно-
фиолетовое окрашивание
(обнаружение пептидных связей)
«Доказательство наличие белка только в живых организмах»
Порядок выполнения.
1. В пробирках находятся свежевыжатый сок картофеля, кусочки сырого картофеля,
вареный картофель.
2. Добавьте в каждую пробирку 2-3 мл перекиси водорода.
3. Отметьте изменения. (каталаза - ферментный белок выделяется только в
присутствии молекулярной воды, растворенные в воде альбумины сворачиваются)
| Опыт | Что делали | Что наблюдали | Объяснение и выводы |
| 1. Качественные реакции на белки. | |||
| а) Биуретовая реакция. | К 2 мл раствора белка добавить раствор сульфата меди (II) и щелочи. | Красно-фиолетовое окрашивание. | При взаимодействии растворов образуется комплексное соединение между ионами Си2+ и полипептидами. |
| б) Ксантопротеиновая реакция. | К 2 мл раствора белка добавить по каплям концентрирующуюся азотную кислоту. | Желтое окрашивание. | Реакция доказывает, что в состав белков входят остатки ароматических аминокислот. |
| 2. Денатурация белка. | Пробирку № 3 с раствором белка нагреть. | Во всех трех случаях наблюдается необратимое свертывание белка — денатурация. | При нагревании, действии неразбавленного спирта, солей тяжелых металлов происходит разрушение вторичной и третичной структуры, с сохранением первичной. |


«Жизнь есть способ существования белковых тел…» Ф.Энгельс
Опорный конспект Приложение № 2- АМФОТЕРНОСТЬ
Кислая среда = по типу щелочи
[белок]+ + ОН- = по типу кислоты
- ГИДРОЛИЗ ……разрушение первичной структуры белка до α-аминлкислот
Качественные реакции
- БИУРЕТОВАЯ РЕАКЦИЯ (распознавание в молекуле белка пептидных связей).
Б. + CuSO4 + NaOH → фиолетовое окрашивание
………………………………
- КСАНТОПРОТЕИНОВАЯ РЕАКЦИЯ (обнаружение бензольных ядер).
Б. + HNO3 → желтое окрашивание
- ГОРЕНИЕ БЕЛКА ………………………..
N2, CO2, H2O - запах жженых перьев
- ДЕНАТУРАЦИЯ - ………………………..
высокая t разрушение
радиоактивное облучение 2-3 структуры
соли тяжелых Ме
Протеины ПротеидыБЕЛКИ - важнейшая составная часть живых организмов, входят в состав кожи, роговых покровов, мышечной и нервной ткани

 (простые) (сложные)
(простые) (сложные)



| 1 вариант | 2 вариант |
| 1. В состав аминокислот входят: а) только аминогруппы б) только карбоксильные группы в) аминогруппы и карбоксильные группы г) аминогруппы и карбонильные группы | 1. Аминокислотой является вещество, формула которого: а) СН3СН2 СОNН2 б) NН2СООН в) NН2СН2СН2СООН г) NН2СН2СОН |
| 2. Аминокислоты, которые не могут синтезироваться в организме человека, а поступают только с пищей, называются а) a -аминокислотами б) пищевыми в) -аминокислотами г) незаменимыми | 2. Аминокислоты - это а) бесцветные легкокипящие жидкости б) газы тяжелее воздуха в) кристаллические вещества розового цвета г) бесцветные кристаллические вещества |
| 3. При взаимодействии аминокислот со щелочами и кислотами образуются: б) сложные эфиры в) дипептиды г) полипептиды | 3. Образование полипептидов происходит по типу реакции: а) полимеризации б) поликонденсации в) присоединения г) замещения |
| 4. Формула 3-аминопропановой кислоты: а) NН2СН2СООН б) NН2СН2СН2СООН в) NН2СН2СН2 NН2 г) NН2СН СН2СООН | 4. Самые слабые кислотные свойства проявляет кислота: а) уксусная б) хлоруксусная в) аминоуксусная г) дихлоруксусная |
| 5. Верным является утверждение, что аминокислоты это: а) твердые вещества молекулярного строения б) кристаллические вещества ионного строения в) жидкости, хорошо растворимые в воде г) кристаллические вещества с низкими температурами плавления | 5. Аминокислоты являются амфотерными соединениями, так как они взаимодействуют: а) с кислотами б) с щелочами в) со спиртами г) с кислотами и щелочами |
Ответы 1 - В, 2 - Г, 3 - А, 4 - Б, 5 - Б Ответы 1 - В, 2 - Г, 3 -Б, 4 -В, 5 - Г
| 1 вариант | 2 вариант |
| 1. Укажите название белка, выполняющего защитную функцию: | 1. Укажите название белка, выполняющего ферментативную функцию: а) гемоглобин, б) оксидаза, в) антитела. |
| 2. Белки - это..: а) полисахариды, б) полипептиды, в) полинуклеотиды. | 2. Биологические свойства белка определяет структура: а) третичная, б) вторичная, в) первичная. |
| 3. Первичная структура белка поддерживается за счёт связей: | 3. Вторичная структура белка поддерживается за счёт связей: а) ионных, б) пептидных, в) водородных. |
| 4. Гидролиз белка используется для: а) получения аминокислот, б) качественного обнаружения белка, в) разрушения третичной структуры | 4. Белки подвергаются реакциям: а) денатурации, б) полимеризации, в) поликонденсации. |
| 5. Аминокислоты, необходимые для построения белков, попадают в организм: а) с водой, б) с пищей, в) с воздухом. | 5. Какой из процессов наиболее сложен: а) микробиологический синтез, б) органический синтез, в) переработка растительного белка. |
Ответы: 1 - в, 2 - б, 3 - б, 4 - а, 5 - б. Ответ: 1 - б, 2 - в, 3 - в. 4 - а, 5 - б.
Тест «Белки»
1 . Какие химические элементы входят в состав белков?
а) углерод б) водород в) кислород г) сера д) фосфор е) азот ё) железо ж) хлор
2 . Сколько аминокислот участвуют в образовании белков?
а) 30 в) 20 б) 26 г) 10
3 . Сколько аминокислот являются незаменимыми для человека?
а) 16 б) 10 в) 20 г) 7
4 . В результате какой реакции образуется пептидная связь?
а) реакция гидролиза в) реакция поликонденсации
б) реакция гидратации г) все вышеперечисленные реакции
5 . Какая функциональная группа придает аминокислоте - кислотные, какая - щелочные свойства? (карбоксильная, аминогруппа).
6 . Какие связи образуют 1- первичную, 2- вторичную, 3- третичную структуры белка? Соотнесите:
а) ковалентные в) ионные
б) водородные г) такие связи отсутствуют
7 ) Определите структуры белковой молекулы:
1.  2.
2.

Таблица ответов
| Номер вопроса | |||||||
| Вариант ответа |
8) Денатурация - это разрушение белка до _____________структуры под действием________________, а также под действием растворов различных химических веществ (______,________, солей) и радиации.
9) Гидролиз - это разрушение _____________структуры белка под действием________________, а так же водных растворов кислот или щелочей.
10) Качественные реакции:
а) Биуретовая.
Белок + ___________________________ = _________________________
б) Ксантопротеиновая.
Белок + ___________________________ = __________________________
11) Установите соответствие между белками и их функцией в организме. Ответ дайте в виде последовательности цифр, соответствующих буквам по алфавиту:
БЕЛКИ: ФУНКЦИЯ:
А) гемоглобин 1)сигнальная
Б) ферменты 2) транспортная
В) антитела и антитоксины 3) структурная
4) каталитическая
5) защитная
12) Заполните значение белков:
| Функции | Значение |
|
| Строительная | Клеточные мембраны, покровные ткани, шерсть, перья, гора, волосы, хрящи |
|
| Транспортная | Накопление и транспорт по организму важнейших веществ |
|
| Энергетическая | Запас аминокислот для развития организма |
|
| Двигательная | Сократительные белки основа мышечных тканей |
|
| Защитная | Белки - антитела, антитоксины распознают и уничтожают бактерии и “чужеродные” вещества |
|
| Каталитическая | Белки - природные катализаторы (ферменты) |
|
| Сигнальная | Мембранные белки воспринимают внешние воздействия и передают сигнал о них внутрь клетки |
Вопросы к брифингу:
Белок иначе называют…
Что является мономерами белка?
Сколько незаменимых АК известно?
Каков атомарный состав белков?
Какая связь поддерживает вторичную структуру?
Как называется связь, образующая ППЦ?
Вторичная структура белковой молекулы в пространстве напоминает…
За счет каких взаимодействий образуются третичная структура?
Почему белки относят к ВМС?
Что в переводе с греческого означает “протеин”?
Что такое “денатурация”?
Как называется процесс взаимодействия белков с Н2О?
Белки, или протеины, - сложные, высокомолекулярные органические соединения, состоящие из аминокислот. Они представляют главную, важнейшую часть всех клеток и тканей животных и растительных организмов, без которой не могут осуществляться жизненно важные физиологические процессы. Белки неодинаковы по своему составу и свойствам в различных животных и растительных организмах и в разных клетках и тканях одного и того же организма. Белки разного молекулярного состава различно растворяются в и в водных солевых растворах, в органических растворителях они не растворяются. Благодаря присутствию в белковой молекуле кислых и основных групп она имеет нейтральную реакцию.
Белки образуют многочисленные соединения с любыми химическими веществами, что обусловливает их особое значение в химических реакциях, протекающих в организме и представляющих основу всех проявлений жизни и защиты ее от вредных воздействий. Белки составляют основу ферментов, антител, гемоглобина, миоглобина, многих гормонов, образуют сложные комплексы с витаминами.
Вступая в соединения с жирами и углеводами, белки могут в организме превращаться при своем расщеплении в жиры и углеводы. В животном организме они синтезируются только из аминокислот и их комплексов – полипептидов, а образовываться из неорганических соединений, жиров и углеводов они не могут. Вне организма синтезированы многие низкомолекулярные биологически активные белковые вещества, сходные с теми, которые имеются в организме, например некоторые гормоны.
Общие сведения о белках и их классификации
Белки - важнейшие биоорганические соединения, которые наряду с нуклеиновыми кислотами занимают особую роль в живом веществе - без этих соединений невозможна жизнь, так как, по определению Ф. Энгельса, жизнь является особым существованием белковых тел и т. д.
«Белки - это природные биополимеры, являющиеся продуктами реакции поликонденсации природных альфа-аминокислот».
Природных альфа-аминокислот 18-23, их сочетание образует бесконечно большое количество разновидностей молекул белков, обеспечивающих многообразие различных организмов. Даже для отдельных особей организмов данного вида характерны свои собственные белки, а ряд белков встречается во многих организмах.
Белки характеризуются следующим элементарным составом: они образованы углеродом, водородом, кислородом, азотом, серой и некоторыми другими химическими элементами. Главной особенностью белковых молекул является обязательное наличие в них азота (помимо атомов С, Н, О).
В молекулах белков реализуется «пептидная» связь, т. е. связь между атомом С карбонильной группы и атомом азота аминогруппы, которая обусловливает некоторые особенности белковых молекул. В боковых цепях молекулы белка содержится большое количество радикалов и функциональных групп, что «делает» молекулу белка полифункциональной, способной к значительному многообразию физико-химических и биохимических свойств.
Из-за большого разнообразия белковых молекул и сложности их состава и свойств, белки имеют несколько различных классификаций, основанных на различных признаках. Рассмотрим некоторые из них.
I. По составу различают две группы белков:
1. Протеины (простые белки; молекула их образована только белком, например яичный альбумин).
2. Протеиды - сложные белки, молекулы которых состоят из белковой и небелковой составляющих.
Протеиды подразделяются на несколько групп, важнейшими из которых являются:
1) гликопротеиды (сложное соединение белка и углевода);
2) липопротеиды (комплекс молекул белка и жиров (липидов);
3) нуклеопротеиды (комплекс белковых молекул и молекул нуклеиновых кислот).
II. По форме молекулы различают две группы белков:
1. Глобулярные белки - молекула белка имеет шарообразную форму (форму глобулы), например молекулы яичного альбумина; такие белки или растворимы в воде, или способны к образованию коллоидных растворов.
2. Фибриллярные белки - молекулы этих веществ имеют форму нитей (фибрилл), например, миозин мышц, фиброин шелка. Фибриллярные белки нерастворимы в воде, они образуют структуры, реализующие сократительную, механическую, формообразующую и защитную функции, а также способность организма передвигаться в пространстве.
III. По растворимости в различных растворителях белки разделяют на несколько групп, из которых наиболее важны следующие:
1. Водорастворимые.
2. Жирорастворимые.
Существуют и другие классификации белков.
Краткая характеристика природных альфа-аминокислот
Природные альфа-аминокислоты являются разновидностью аминокислот. Аминокислота - полифункциональное органическое вещество, содержащее в своем составе как минимум две функциональные группы - аминогруппу (-NН 2) и карбоксильную (карбоксидную, последнее правильнее) группу (-СООН).
Альфа-аминокислоты - такие аминокислоты, в молекулах которых амино- и карбоксильные группы находятся у одного атома углерода. Их общая формула - NН 2 СН(R)СООН. Ниже приведены формулы некоторых природных альфа-аминокислот; они записаны в виде, удобном для написания уравнений реакции поликонденсации и используются в случае, когда необходимо написать уравнения (схемы) реакций получения определенных полипептидов:
1) глицин (аминоуксусная кислота) - МН 2 СН 2 СООН;
2) аланин — NН 2 СН(СН 3)СООН;
3) фенилаланин — NН 2 СН(СН 2 С 6 Н 5)СООН;
4) серин — NН 2 СН(СН 2 ОН)СООН;
5) аспарагиновая кислота - NН 2 СН(СН 2 СООН)СООН;
6) цистеин — NН 2 СН(СН 2 SН)СООН и т.д.
Некоторые природные альфа-аминокислоты содержат по две аминогруппы (например, лизин), по две карбоксидные группы (например, аспарагиновая и глутаминовые кислоты), гидроксидные (ОН) группы (например, тирозин), могут быть циклическими (например, пролин).
По характеру влияния природных альфа-аминокислот на обмен веществ их разделяют на заменимые и незаменимые. Незаменимые аминокислоты должны обязательно поступать в организм с пищей.
Краткая характеристика структуры молекул белка
Белки кроме сложного состава характеризуются и сложным строением белковых молекул. Различают четыре вида структур белковых молекул.
1. Первичная структура характеризуется порядком расположения остатков альфа-аминокислот в полипептидной цепи. Например, тетрапептид (полипептид, образовавшийся при поликонденсации четырех молекул аминокислоты) ала-фен-тиро-серин представляет собой последовательность остатков аланина, фенилаланина, тирозина и серина, связанных друг с другом пептидной связью.
2. Вторичная структура белковой молекулы представляет собой пространственное расположение полипептидной цепи. Оно бывает различным, но наиболее распространенной является альфа-спираль, характеризующаяся определенным «шагом» спирали, размерами и расстоянием между отдельными витками спирали.
Устойчивость вторичной структуры белковой молекулы обеспечивается возникновением различных химических связей между отдельными витками спирали. Важнейшая роль среди них принадлежит водородной связи (реализуется за счет втягивания ядра атома групп - NH 2 или =NH в электронную оболочку атомов кислорода или азота), ионной связи (реализуется за счет электростатического взаимодействия ионов -СОО — и - NH + 3 или =NH + 2) и других видов связи.
3. Третичная структура молекул белка характеризуется пространственным расположением альфа-спирали, или иной структуры. Устойчивость таких структур обусловливается теми же видами связи, что и вторичная структура. В результате реализации третичной структуры возникает «субъединица» белковой молекулы, что характерно для очень сложных молекул, а для относительно простых молекул третичная структура является конечной.
4. Четвертичная структура белковой молекулы представляет собой пространственное расположение субъединиц молекул белка. Она характерна для сложных белков, например гемоглобина.
Рассматривая вопрос о структуре белковых молекул, необходимо различать структуру живого белка - нативную структуру и структуру мертвого белка. Белок в живом веществе (нативный белок) отличается от белка, подвергшегося воздействию, при котором он может потерять свойства живого белка. Неглубокое воздействие называют денатурацией, при которой в дальнейшем свойства живого белка могут восстанавливаться. Одним из видов денатурации является обратимая коагуляция. При необратимой коагуляции нативный белок превращается в «мертвый белок».
Краткая характеристика физических, физико-химических и химических свойств белка
Свойства белковых молекул имеют большое значение для реализации их биолого-экологических свойств. Так, по агрегатному состоянию белки относят к твердым веществам, которые могут быть растворимыми или нерастворимыми в воде или других растворителях. Многое в биоэкологической роли белков определяется физическими свойствами. Так, способность молекул белка образовывать коллоидные системы обусловливает их строительную, каталитическую и другие функции. Нерастворимость белков в воде и других растворителях, их фибриллярность обусловливает защитную и формообразующую функции и т. д.
К физико-химическим свойствам белков относится их способность к денатурации и коагуляции. Коагуляция проявляется в коллоидных системах, которые являются основой любого живого вещества. При коагуляции частицы укрупняются за счет их слипания. Коагуляция бывает скрытой (ее можно наблюдать только под микроскопом) и явной - ее признаком является выпадение осадка белка. Коагуляция бывает необратимой, когда после прекращения действия коагулирующего фактора структура коллоидной системы не восстанавливается, и обратимой, когда после удаления коагулирующего фактора коллоидная система восстанавливается.
Примером обратимой коагуляции является выпадение белка яичного альбумина под действием растворов солей, при этом осадок белка растворяется при разбавлении раствора либо при перенесении осадка в дистиллированную воду.
Примером необратимой коагуляции является разрушение коллоидной структуры белка альбумина при нагревании до температуры кипения воды. При смерти (полной) живое вещество превращается в мертвое за счет необратимой коагуляции всей системы.
Химические свойства белков весьма многообразны из-за наличия в белковых молекулах большого числа функциональных групп, а также за счет наличия пептидной и других связей в молекулах белка. С эколого-биологических позиций наибольшее значение имеет способность молекул белка к гидролизу (при этом в конечном счете получается смесь природных альфа-аминокислот, которые участвовали в образовании данной молекулы, в этой смеси могут быть и другие вещества, если белок был протеидом), к окислению (его продуктами могут быть углекислый газ, вода, соединения азота, например, мочевина, соединения фосфора и т. д.).
Белки горят с выделением запаха «жженого рога» или «жженых перьев», что необходимо знать при проведении экологических опытов. Известны различные цветные реакции на белок (биуретова, ксантопротеиновая и др.), подробнее о них - в курсе химии.
Краткая характеристика эколого-биологических функций белков
Необходимо различать эколого-биологическую роль белков в клетках и в организме в целом.
Эколого-биологическая роль белков в клетках
Вследствие того, что белки (наряду с нуклеиновыми кислотами) - это вещества жизни, то их функции в клетках весьма многообразны.
1. Важнейшей функцией белковых молекул является структурная функция, состоящая в том, что белок - это важнейший компонент всех структур, образующих клетку, в которые он входит в составе комплекса различных химических соединений.
2. Белок - важнейший реагент в протекании огромного многообразия биохимических реакций, обеспечивающих нормальное функционирование живого вещества, поэтому для него характерна реагентная функция.
3. В живом веществе реакции возможны только в присутствии биологических катализаторов - ферментов, а как установлено в результате биохимических исследований, имеют белковую природу, поэтому белки выполняют и каталитическую функцию.
4. В случае необходимости в организмах белки окисляются и при этом выделяется , за счет которой синтезируется АТФ, т.е. белки выполняют и энергетическую функцию, но вследствие того, что эти вещества имеют для организмов особую ценность (из-за их сложного состава), то энергетическая функция белков реализуется организмами только в критических условиях.
5. Белки могут выполнять и запасающую функцию, так как являются своеобразными «консервами» веществ и энергии для организмов (особенно растений), обеспечивающих их начальное развитие (для животных - внутриутробное, для растений - развитие зародышей до появления молодого организма - проростка).
Ряд функций белка характерны и для клеток, и для организма в целом, поэтому рассмотрены ниже.
Эколого-биологическая роль белков в организмах (в целом)
1. Белки образуют в клетках и организмах особые структуры (в совокупности с другими веществами), которые способны воспринимать сигналы из окружающей среды в виде раздражений, за счет чего возникает состояние «возбуждения», на которое организм отвечает определенной реакцией, т.е. для белков и в клетке, и в организме в целом характерна воспринимающая функция.
2. Белкам характерна и проводящая функция (и в клетках, и в организме в целом), состоящая в том, что возникшее в определенных структурах клетки (организма) возбуждение, передается в соответствующий центр (клетки или организма), в котором формируется определенная реакция (ответ) организма или клетки на поступивший сигнал.
3. Многие организмы способны к перемещению в пространстве, что возможно за счет способности структур клетки или организма к сокращению, а это возможно потому, что белки фибриллярной структуры обладают сократительной функцией.
4. Для гетеротрофных организмов белки как отдельно, так и в смеси с другими веществами являются продуктами питания, т. е. им характерна трофическая функция.
Краткая характеристика превращений белков в гетеротрофных организмах на примере человека
Белки в составе пищи попадают в ротовую полость, где смачиваются слюной, измельчаются зубами и превращаются в гомогенную массу (при тщательном пережевывании), и через глотку и пищевод поступают в желудок (до попадания в последний с белками как соединениями ничего не происходит).
В желудке пищевой комок пропитывается желудочным соком, являющимся секретом желудочных желез. Желудочный сок представляет собой водную систему, содержащую хлороводород и ферменты, важнейшим из которых (для белков) является пепсин. Пепсин в кислой среде вызывает процесс гидролиза белков до пептонов. Пищевая кашица далее поступает в первый отдел тонкого кишечника - двенадцатиперстную кишку, в которую открывается проток поджелудочной железы, выделяющей панкреатический сок, обладающий щелочной средой и комплексом ферментов, из которых трипсин ускоряет процесс гидролиза белков и ведет его до конца, т. е. до появления смеси природных альфа-аминокислот (они растворимы и способны всасываться в кровь ворсинками кишечника).
Эта смесь аминокислот поступает в межтканевую жидкость, а оттуда - в клетки организма, в которых они (аминокислоты) вступают в различные превращения. Одна часть этих соединений непосредственно используется для синтеза белков, характерных для данного организма, вторая - подвергается переаминированию или дезаминированию, давая новые соединения, необходимые организму, третья - окисляется и является источником энергии, необходимой организму для реализации своих жизненных функций.
Необходимо отметить некоторые особенности внутриклеточных превращений белков. Если организм гетеротрофный и одноклеточный, то белки в составе пищи попадают внутрь клеток в цитоплазму или специальные пищеварительные вакуоли, где под действием ферментов подвергаются гидролизу, а далее все протекает так, как описано для аминокислот в клетках. Клеточные структуры постоянно обновляются, поэтому «старый» белок заменяется на «новый», при этом первый гидролизуется с получением смеси аминокислот.
У автотрофных организмов имеются свои особенности в превращениях белков. Первичные белки (в клетках меристем) синтезируются из аминокислот, которые синтезируются из продуктов превращений первичных углеводов (они возникли при фотосинтезе) и неорганических азотсодержащих веществ (нитратов или солей аммония). Замена белковых структур в длительно живущих клетках автотрофных организмов не отличается от такового для гетеротрофных организмов.
Азотистое равновесие
Белки, состоящие из аминокислот, - это основные соединения, которым свойственны процессы жизни. Поэтому исключительно важен учет обмена белков и продуктов их расщепления.
Азота в составе пота очень мало, поэтому обычно анализ пота на содержание азота не делается. Количество азота, поступившего с пищей, и количество азота, содержащегося в моче и кале, умножается на 6,25 (16%) и из первой величины вычитается вторая. В результате определяется количество азота, поступившего в организм и усвоенного им.
Когда поступившее в организм с пищей количество азота равно количеству азота в моче и кале, т. е. образовавшемуся при дезаминировании, то имеется азотистое равновесие. Азотистое равновесие свойственно, как правило, взрослому здоровому организму.
Когда количество поступившего в организм азота больше количества выделенного азота, то имеется положительный азотистый баланс, т. е. количество белка, вошедшего в состав организма, больше количества белка, подвергшегося распаду. Положительный азотистый баланс характерен для растущего здорового организма.
Когда поступление белка с пищей увеличивается, то увеличивается и количество азота, выделяемого с мочой.
И, наконец, когда количество поступившего в организм азота меньше количества выделенного азота, то имеется отрицательный азотистый баланс, при котором распад белка превышает его синтез и разрушается белок, входящий в состав организма. Это бывает при белковом голодании и тогда, когда не поступают необходимые для организма аминокислоты. Отрицательный азотистый баланс обнаружен и после действия больших доз ионизирующего облучения, вызывающих усиленный распад белков в органах и тканях.
Проблема белкового оптимума
Минимальное количество белков пищи, необходимое для восполнения разрушающихся белков организма, или величина распада белков организма при исключительно углеводном питании, обозначается как коэффициент изнашивания. У взрослого человека наименьшая величина этого коэффициента около 30 г белков в сутки. Однако этого количества недостаточно.
Жиры и углеводы оказывают влияние на расход белков сверх минимума, необходимого для пластических целей, так как они освобождают то количество энергии, которое требовалось для расщепления белков сверх минимума. Углеводы при нормальном питании уменьшают расщепление белков в 3-3,5 раза больше, чем при полном голодании.
Для взрослого человека при смешанной пище, содержащей достаточное количество углеводов и жиров, и массе тела 70 кг норма белка в сутки равна 105 г.
Количество белка, полностью обеспечивающее рост и жизнедеятельность организма, обозначается как белковый оптимум и равно у человека при легкой работе 100-125 г белка в сутки, при тяжелой работе - до 165 г, а при очень тяжелой - 220-230 г.
Количество белка в сутки должно быть по массе не меньше 17% от общего количества пищи, а по энергии - 14%.
Полноценные и неполноценные белки
Белки, поступающие в организм с пищей, разделяются на биологически полноценные и биологически неполноценные.
Биологически полноценными называются те белки, в которых в достаточном количестве содержатся все аминокислоты, необходимые для синтеза белка животного организма. В состав полноценных белков, необходимых для роста организма, входят следующие незаменимые аминокислоты: лизин, триптофан, треонин, лейцин, изолейцин, гистидин, аргинин, валин, метионин, фенилаланин. Из этих аминокислот могут образоваться другие аминокислоты, гормоны и т. д. Из фенилаланина образуется тирозин, из тирозина путем превращений - гормоны тироксин и адреналин, из гистидина - гистамин. Метионин участвует в образовании гормонов щитовидной железы и необходим для образования холина, цистеина и глютатиона. Он необходим для окислительно-восстановительных процессов, азотистого обмена, усвоения жиров, нормальной деятельности головного мозга. Лизин участвует в кроветворении, способствует росту организма. Триптофан также необходим для роста, участвует в образовании серотонина, витамина РР, в тканевом синтезе. Лизин, цистин и валин возбуждают сердечную деятельность. Малое содержание цистина в пище задерживает рост волос, увеличивает содержание сахара в крови.
Биологические неполноценными называются те белки, в которых отсутствуют хотя бы даже одна аминокислота, которая не может быть синтезирована животными организмами.
Биологическая ценность белка измеряется количеством белка организма, которое образуется из 100 г белка пищи.
Белки животного происхождения, содержаться в мясе, яйцах и молоке, наиболее полоненные (70-95%). Белки растительного происхождения имеют меньшую биологическую ценность, например белки ржаного хлеба, кукурузы (60%), картофеля, дрожжей (67%).
Белок животного происхождения – желатина, в котором нет триптофана и тирозина, является неполноценным. В пшенице и ячмене мало лизина, в кукурузе мало лизина и триптофана.
Некоторые аминокислоты заменяют друг друга, например фенилаланин заменяет тирозин.
Два неполноценных белка, в которых недостает разлчных аминокислот, вместе могут составить полноценное белковое питание.
Роль печени в синтезе белков
В печени синтезируются белки, содержащиеся в плазме крови: альбумины, глобулины (за исключением гамма-глобулинов), фибриноген, нуклеиновые кислоты и многочисленные ферменты, из которых некоторые синтезируются только в печени, например ферменты, участвующие в образовании мочевины.
Белки, синтезированные в организме, входят в состав органов, тканей и клеток, ферментов и гормонов (пластическое значение белков), но не запасаются организмом в виде разных белковых соединений. Поэтому та часть белков, которая не имеет пластического значения, при участии ферментов дезаминируется – распадается с освобождением энергии на разные азотистые продукты. Период полураспада белков печени равен 10 дням.
Белковое питание при различных условиях
Нерасщепленный белок не может быть усвоен организмом иначе, как через пищеварительный канал. Белок, введенный вне пищеварительного канала (парэнтерально), вызывает защитную реакцию со стороны организма.
Аминокислоты расщепленного белка и их соединения – полипептиды – приносятся к клеткам организма, в которых под влиянием ферментов непрерывно в течении всей жизни происходит синтез белков. Белки пищи имеют главным образом пластическое значение.
В период роста организма – в детском и юношеском возрасте – синтез белков особенно велик. В старости синтез белков уменьшается. Следовательно, в процессе роста происходит ретенция, или задержка в организме химических , из которых состоят белки.
Изучение обмена с применением изотопов показало, что в некоторых органах в течение 2-3 суток приблизительно половина всех белков подвергается распаду и такое же количество белков заново синтезируется организмом (ресинтез). В каждой , в каждом организме синтезируются специфические белки, отличающиеся от белков других тканей и других организмов.
Подобно жирам и углеводам, аминокислоты, не использованные для построения организма, подвергаются распаду с освобождением энергии.
Аминокислоты, которые образуются из белков умирающих, разрушающихся клеток организма, также подвергаются превращениям с освобождением энергии.
В обычных условиях количество необходимого белка в сутки для взрослого человека 1,5-2,0 г на 1 кг массы тела, в условиях длительного холода 3,0-3,5 г, при очень тяжелой физической работе 3,0-3,5 г.
Увеличение количества белков больше чем до 3,0-3,5 г на 1 кг массы тела нарушает деятельность нервной системы, печени и почек.
Липиды, их классификация и физиологическая роль
Липиды - вещества, нерастворимые в воде и растворяющиеся в органических соединениях (спирте, хлороформе и др.). К липидам относятся нейтральные жиры, жироподобные вещества (липоиды) и некоторые витамины (A, D, E, K). Липиды имеют пластическое значение и входят в состав всех клеток и половых гормонов.
Особенно много липидов в клетках нервной системы и надпочечниках. Значительная часть их используется организмом как энергетический материал.
Аминокислоты В состав природных полипептидов и белков входят аминокислоты, в молекулах которых амино и карбоксильная группы связаны с одним и тем же атомом углерода. H 2 N–СН–СООН R В зависимости от строения углеводородного радикала R природные аминокислоты разделяют на алифатические, ароматические и гетероциклические. Алифатические аминокислоты могут быть неполярными (гидрофобными), полярными незаряженными и полярными заряженными. В зависимости от содержания функциональных групп в радикале выделяют аминокислоты, содержащие гидроксильную, амидную, карбоксильную и аминогруппы. Обычно используются тривиальные названия аминокислот, которые обычно связаны с источниками их выделения или свойствами.
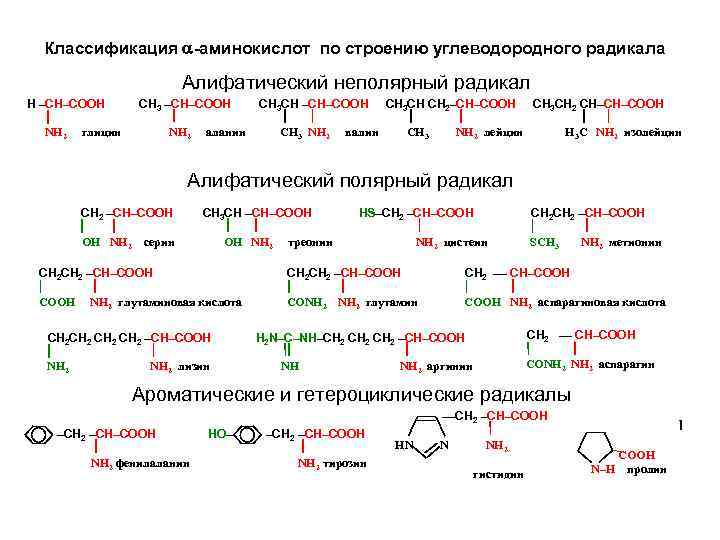 Классификация -аминокислот по строению углеводородного радикала Алифатический неполярный радикал Н –СН–СООН NH 2 СН 3 –СН–СООН глицин NH 2 СН 3 СН –СН–СООН СН 3 NH 2 аланин СН 3 СН СН 2–СН–СООН валин СН 3 СН 2 СН–СН–СООН Н 3 С NH 2 изолейцин NH 2 лейцин Алифатический полярный радикал СН 2 –СН–СООН ОН NH 2 НS–СН 2 –СН–СООН СН 3 СН –СН–СООН серин ОН NH 2 СН 2 –СН–СООН NH 2 цистеин треонин SСН 3 NH 2 метионин СН 2 СН 2 –СН–СООН СН 2 –– СН–СООН СОNН 2 NH 2 глутамин СООН NH 2 аспарагиновая кислота NH 2 глутаминовая кислота СН 2 –СН–СООН NН 2 NH 2 лизин СН 2 –– СН–СООН H 2 N–С–NН–СН 2 –СН–СООН NН СОNН 2 NH 2 аспарагин NH 2 аргинин Ароматические и гетероциклические радикалы ––СН –СН–СООН Гетероциклический радикал –СН–СООН НО– –СН–СООН HN N NH СООН Карбоциклический радикал тирозин NH фенилаланин NH 2 2 2 гистидин N–H пролин
Классификация -аминокислот по строению углеводородного радикала Алифатический неполярный радикал Н –СН–СООН NH 2 СН 3 –СН–СООН глицин NH 2 СН 3 СН –СН–СООН СН 3 NH 2 аланин СН 3 СН СН 2–СН–СООН валин СН 3 СН 2 СН–СН–СООН Н 3 С NH 2 изолейцин NH 2 лейцин Алифатический полярный радикал СН 2 –СН–СООН ОН NH 2 НS–СН 2 –СН–СООН СН 3 СН –СН–СООН серин ОН NH 2 СН 2 –СН–СООН NH 2 цистеин треонин SСН 3 NH 2 метионин СН 2 СН 2 –СН–СООН СН 2 –– СН–СООН СОNН 2 NH 2 глутамин СООН NH 2 аспарагиновая кислота NH 2 глутаминовая кислота СН 2 –СН–СООН NН 2 NH 2 лизин СН 2 –– СН–СООН H 2 N–С–NН–СН 2 –СН–СООН NН СОNН 2 NH 2 аспарагин NH 2 аргинин Ароматические и гетероциклические радикалы ––СН –СН–СООН Гетероциклический радикал –СН–СООН НО– –СН–СООН HN N NH СООН Карбоциклический радикал тирозин NH фенилаланин NH 2 2 2 гистидин N–H пролин
 Заменимые и незаменимые -аминокислоты Все природные аминокислоты делят на незаменимые, которые поступают в организм только из внешней среды, и заменимые, синтез которых происходит в организме. Незаменимые аминокислоты: Заменимые аминокислоты: валин, лейцин, изолейцин, глицин, аланин, пролин, лизин, метионин, треонин, серин, цистеин, аргинин, гистидин, триптофан, фенилаланин аспарагин, глутамин, аспарагиновая и глутаминовая кислоты В качестве исходных веществ при биосинтезе аминокислот могут выступать другие аминокислоты, а также вещества, относящиеся к другим классам органических соединений (например, кетокислоты) Катализаторами и участниками этого процесса являются ферменты. Анализ аминокислотного состава различных белков показывает, что на долю дикарбоновых кислот и их амидов в большинстве белков приходится 25 27 % всех аминокислот. Эти же аминокислоты вместе с лейцином и лизином составляют около 50 % всех аминокислот белков. В то же время на долю таких аминокислот, как цистеин, метионин, триптофан, гистидин приходится не более 1, 5 – 3, 5 %.
Заменимые и незаменимые -аминокислоты Все природные аминокислоты делят на незаменимые, которые поступают в организм только из внешней среды, и заменимые, синтез которых происходит в организме. Незаменимые аминокислоты: Заменимые аминокислоты: валин, лейцин, изолейцин, глицин, аланин, пролин, лизин, метионин, треонин, серин, цистеин, аргинин, гистидин, триптофан, фенилаланин аспарагин, глутамин, аспарагиновая и глутаминовая кислоты В качестве исходных веществ при биосинтезе аминокислот могут выступать другие аминокислоты, а также вещества, относящиеся к другим классам органических соединений (например, кетокислоты) Катализаторами и участниками этого процесса являются ферменты. Анализ аминокислотного состава различных белков показывает, что на долю дикарбоновых кислот и их амидов в большинстве белков приходится 25 27 % всех аминокислот. Эти же аминокислоты вместе с лейцином и лизином составляют около 50 % всех аминокислот белков. В то же время на долю таких аминокислот, как цистеин, метионин, триптофан, гистидин приходится не более 1, 5 – 3, 5 %.
 Стереоизомерия -аминокислот Пространственные или стереоизомеры или оптически активные соединения – соединения, способные существовать в пространстве в виде двух изомеров, являющихся зеркальным отражением друга (энантиомеры). Все -аминокислоты, кроме глицина, являются оптически активными соединениями и способны вращать плоскость поляризации плоскополяризованного света (все волны которого колеблются в одной плоскости) вправо (+, правовращающие) или влево (-, левовращающие). Признаки оптической активности: - наличие в молекуле асимметричного атома углерода (атома, связанного с четырьмя разными заместителями); - отсутствие в молекуле элементов симметрии. Энантиомеры -аминокислот обычно изображают в виде относительной конфигурации и называют по D, L-номенклатуре.
Стереоизомерия -аминокислот Пространственные или стереоизомеры или оптически активные соединения – соединения, способные существовать в пространстве в виде двух изомеров, являющихся зеркальным отражением друга (энантиомеры). Все -аминокислоты, кроме глицина, являются оптически активными соединениями и способны вращать плоскость поляризации плоскополяризованного света (все волны которого колеблются в одной плоскости) вправо (+, правовращающие) или влево (-, левовращающие). Признаки оптической активности: - наличие в молекуле асимметричного атома углерода (атома, связанного с четырьмя разными заместителями); - отсутствие в молекуле элементов симметрии. Энантиомеры -аминокислот обычно изображают в виде относительной конфигурации и называют по D, L-номенклатуре.
 Относительные конфигурации -аминокислот В молекуле аланина второй атом углерода является асимметричным (у него 4 разных заместителя: атом водорода, карбоксильная, метильная и аминогруппы. Углеводородную цепь молекулы располагают вертикально, в зеркальном отражении изображают только атомы и группы, связанные с асимметричным атомом углерода. Для аминокислот это, как правило, атом водорода и аминогруппа. Если аминогруппа располагается справа от углеродной цепи, это D изомер; если слева – L изомер. СООН Н–С– NH 2 СН 3 D-аланин СООН H 2 N–С– Н СН 3 L-аланин В состав природных белков входят только L изомеры аминокислот. Относительная конфигурация не определяет направление вращения плоскости поляризации плоскополяризованного света. Чуть больше половины L аминокислот являются правовращающими (аланин, изолейцин, глутаминовая кислота, лизин и др.); немного меньше левовращающих кислот (фенилаланин, триптофан, лейцин и др.)
Относительные конфигурации -аминокислот В молекуле аланина второй атом углерода является асимметричным (у него 4 разных заместителя: атом водорода, карбоксильная, метильная и аминогруппы. Углеводородную цепь молекулы располагают вертикально, в зеркальном отражении изображают только атомы и группы, связанные с асимметричным атомом углерода. Для аминокислот это, как правило, атом водорода и аминогруппа. Если аминогруппа располагается справа от углеродной цепи, это D изомер; если слева – L изомер. СООН Н–С– NH 2 СН 3 D-аланин СООН H 2 N–С– Н СН 3 L-аланин В состав природных белков входят только L изомеры аминокислот. Относительная конфигурация не определяет направление вращения плоскости поляризации плоскополяризованного света. Чуть больше половины L аминокислот являются правовращающими (аланин, изолейцин, глутаминовая кислота, лизин и др.); немного меньше левовращающих кислот (фенилаланин, триптофан, лейцин и др.)
 Конфигурация аминокислот определяет пространственную структуру и биологические свойства как самих аминокислот, биополимеров – белков, которые построены из остатков аминокислот. Для некоторых аминокислот наблюдается связь между их конфигурацией и вкусом, например L Tрп, L Фен, L Tир, L Лей имеют горький вкус, а их D энантиомеры сладкие. Сладкий вкус глицина известен давно. L изомер треонина одним людям кажется сладким, другим – горьким. Мононатриевая соль глутаминовой кислоты глутамат натрия один из важнейших носителей вкусовых качеств, применяемых в пищевой промышленности. Интересно заметить, что производное дипептида из аспарагиновой кислоты и фенилаланина обнаруживает интенсивно сладкий вкус. Все аминокислоты представляют собой белые кристаллические вещества, имеющие очень высокие температуры правления (более 230 °С). Большинство кислот хорошо растворимы в воде и практически не растворимы в спирте и диэтиловом эфире. Это, так же как и высокая температура плавления, указывает на солеобразный характер этих веществ. Специфическая растворимость аминокислот обусловлена наличием в молекуле одновременно аминогруппы (основный характер) и карбоксильной группы (кислотные свойства), благодаря чему аминокислоты принадлежат к амфотерным электролитам (амфолитам).
Конфигурация аминокислот определяет пространственную структуру и биологические свойства как самих аминокислот, биополимеров – белков, которые построены из остатков аминокислот. Для некоторых аминокислот наблюдается связь между их конфигурацией и вкусом, например L Tрп, L Фен, L Tир, L Лей имеют горький вкус, а их D энантиомеры сладкие. Сладкий вкус глицина известен давно. L изомер треонина одним людям кажется сладким, другим – горьким. Мононатриевая соль глутаминовой кислоты глутамат натрия один из важнейших носителей вкусовых качеств, применяемых в пищевой промышленности. Интересно заметить, что производное дипептида из аспарагиновой кислоты и фенилаланина обнаруживает интенсивно сладкий вкус. Все аминокислоты представляют собой белые кристаллические вещества, имеющие очень высокие температуры правления (более 230 °С). Большинство кислот хорошо растворимы в воде и практически не растворимы в спирте и диэтиловом эфире. Это, так же как и высокая температура плавления, указывает на солеобразный характер этих веществ. Специфическая растворимость аминокислот обусловлена наличием в молекуле одновременно аминогруппы (основный характер) и карбоксильной группы (кислотные свойства), благодаря чему аминокислоты принадлежат к амфотерным электролитам (амфолитам).
 Кислотно-основные свойства -аминокислот В аминокислотах одновременно присутствует как кислотная карбоксильная группа, так и основная аминогруппа. В водных растворах и твердом состоянии аминокислоты существуют только в виде внутренних солей – цвиттер ионов или биполярных ионов. Кислотно основное равновесие для аминокислоты может быть описано: СН 3 –СН–СОО - ОН– NH 2 Н+ анион СН 3 –СН–СОО– Н+ +NH 3 биполярный ОН- ион СН 3 –СН–СООН +NH 3 катион В кислой среде молекулы аминокислот представляют собой катион. При пропускании электрического тока через такой раствор катионы аминокислот движутся к катоду и там восстанавливаются. В щелочной среде молекулы аминокислот представляют собой анион. При пропускании электрического тока через такой раствор анионы аминокислот движутся к аноду и там окисляются. Значение р. Н, при котором практически все молекулы аминокислоты представляют собой биполярный ион называется изоэлектрической точкой (р. I). При этом значении р. Н раствор аминокислоты не проводит электрический ток.
Кислотно-основные свойства -аминокислот В аминокислотах одновременно присутствует как кислотная карбоксильная группа, так и основная аминогруппа. В водных растворах и твердом состоянии аминокислоты существуют только в виде внутренних солей – цвиттер ионов или биполярных ионов. Кислотно основное равновесие для аминокислоты может быть описано: СН 3 –СН–СОО - ОН– NH 2 Н+ анион СН 3 –СН–СОО– Н+ +NH 3 биполярный ОН- ион СН 3 –СН–СООН +NH 3 катион В кислой среде молекулы аминокислот представляют собой катион. При пропускании электрического тока через такой раствор катионы аминокислот движутся к катоду и там восстанавливаются. В щелочной среде молекулы аминокислот представляют собой анион. При пропускании электрического тока через такой раствор анионы аминокислот движутся к аноду и там окисляются. Значение р. Н, при котором практически все молекулы аминокислоты представляют собой биполярный ион называется изоэлектрической точкой (р. I). При этом значении р. Н раствор аминокислоты не проводит электрический ток.
 Значения p. I важнейших α-аминокислот Цистеин (Cys) Аспарагин (Asp) Фенилаланин (Phe) Треонин (Thr) Глутамин (Gln) Серин (Ser) Тирозин (Tyr) Метионин (Met) Триптофан (Trp) Аланин (Ala) Валин (Val) Глицин (Gly) Лейцин (Leu) Изолейцин (Ile) Пролин (Pro) 5, 0 5, 4 5, 5 5, 6 5, 7 5, 8 5, 9 6, 0 6, 1 6, 3 Аспарагиновая кислота (Asp) Глутаминовая кислота (Glu) Гистидин (His) Лизин (Lys) Аргинин (Arg) 3, 0 3, 2 7, 6 9, 8 10, 8
Значения p. I важнейших α-аминокислот Цистеин (Cys) Аспарагин (Asp) Фенилаланин (Phe) Треонин (Thr) Глутамин (Gln) Серин (Ser) Тирозин (Tyr) Метионин (Met) Триптофан (Trp) Аланин (Ala) Валин (Val) Глицин (Gly) Лейцин (Leu) Изолейцин (Ile) Пролин (Pro) 5, 0 5, 4 5, 5 5, 6 5, 7 5, 8 5, 9 6, 0 6, 1 6, 3 Аспарагиновая кислота (Asp) Глутаминовая кислота (Glu) Гистидин (His) Лизин (Lys) Аргинин (Arg) 3, 0 3, 2 7, 6 9, 8 10, 8
 Химические свойства -аминокислот Реакции с участием карбоксильной группы Реакции с участием аминогруппы Реакции с участием углеводородного радикала кислоты Реакции с одновременным участием карбоксильной и аминогруппы
Химические свойства -аминокислот Реакции с участием карбоксильной группы Реакции с участием аминогруппы Реакции с участием углеводородного радикала кислоты Реакции с одновременным участием карбоксильной и аминогруппы
 Реакции с участием карбоксильной группы -аминокислот Аминокислоты могут вступать в те же химические реакции и давать те же производные, что и другие карбоновые кислоты. СН 3 –СН–СООН Na. OH СН 3 –СН–СООNa NH 2 СН 3 –СН–СООН NH 2 СН 3 ОН NН 3 NH 2 t NH 2 СН 3 –СН–СОNН 2 NH 2 амид аланина Одна из важнейших реакций в организме – декарбоксилирование аминокислот. При отщеплении СО 2 под действием особых ферментов декарбоксилаз аминокислоты превращаются в амины: СН 2 –СН–СООН NH 2 глутаминовая кислота + H 2 O метиловый эфир аланина СН 3 –СН–СОО– NН 4+ NH 2 СН 3 –СН–СООСН 3 Н+ СН 3 –СН–СООН + H 2 O натриевая соль аланина СН 2 –СН 2 NH 2 –СО 2 -аминомасляная кислота (ГАМК) выступает в роли нейромедиатора СООН Реакции по углеводородному радикалу: окисление, а точнее гидроксилирование фенилаланина: –СН 2 –СН–СООН NH 2 фенилаланин [O] НО– –СН 2 –СН–СООН NH 2 тирозин
Реакции с участием карбоксильной группы -аминокислот Аминокислоты могут вступать в те же химические реакции и давать те же производные, что и другие карбоновые кислоты. СН 3 –СН–СООН Na. OH СН 3 –СН–СООNa NH 2 СН 3 –СН–СООН NH 2 СН 3 ОН NН 3 NH 2 t NH 2 СН 3 –СН–СОNН 2 NH 2 амид аланина Одна из важнейших реакций в организме – декарбоксилирование аминокислот. При отщеплении СО 2 под действием особых ферментов декарбоксилаз аминокислоты превращаются в амины: СН 2 –СН–СООН NH 2 глутаминовая кислота + H 2 O метиловый эфир аланина СН 3 –СН–СОО– NН 4+ NH 2 СН 3 –СН–СООСН 3 Н+ СН 3 –СН–СООН + H 2 O натриевая соль аланина СН 2 –СН 2 NH 2 –СО 2 -аминомасляная кислота (ГАМК) выступает в роли нейромедиатора СООН Реакции по углеводородному радикалу: окисление, а точнее гидроксилирование фенилаланина: –СН 2 –СН–СООН NH 2 фенилаланин [O] НО– –СН 2 –СН–СООН NH 2 тирозин
 Реакции с участием аминогруппы -аминокислот Как и другие алифатические амины, аминокислоты могут реагировать с кислотами, ангидридами и хлорангидридами кислот, азотистой кислотой. СН 3 –СН–СООН HCl СН 3 –СН–СООH NH 2 +NH СН 3 –СН–СООН NH 2 СН 3 СОCl –HCl СН 33–СН–СООН СН –СН–СООН 3 Cl– хлорид аланина СН 3 –СН–СООH NH–СО–СН 3 HNO 22 HNO кислота 2 -ацетиламинопропановая СН 33–СН–СООH СН –СН–СООH + N 22+ H 22 O + N + HO OH 2 -гидроксипропановая кислота NH 22 NH При нагревании аминокислот происходит реакция межмолекулярной дегидратации с участием как амино, так и карбоксильной группы. В результате образуется циклический дикетопиперазин. 2 СН 3 –СН–СООН NH 2 t – 2 Н 2 О СН 3 –СН–СО–NH HN––CO–CH–CH 3 дикетопиперазин аланина
Реакции с участием аминогруппы -аминокислот Как и другие алифатические амины, аминокислоты могут реагировать с кислотами, ангидридами и хлорангидридами кислот, азотистой кислотой. СН 3 –СН–СООН HCl СН 3 –СН–СООH NH 2 +NH СН 3 –СН–СООН NH 2 СН 3 СОCl –HCl СН 33–СН–СООН СН –СН–СООН 3 Cl– хлорид аланина СН 3 –СН–СООH NH–СО–СН 3 HNO 22 HNO кислота 2 -ацетиламинопропановая СН 33–СН–СООH СН –СН–СООH + N 22+ H 22 O + N + HO OH 2 -гидроксипропановая кислота NH 22 NH При нагревании аминокислот происходит реакция межмолекулярной дегидратации с участием как амино, так и карбоксильной группы. В результате образуется циклический дикетопиперазин. 2 СН 3 –СН–СООН NH 2 t – 2 Н 2 О СН 3 –СН–СО–NH HN––CO–CH–CH 3 дикетопиперазин аланина
 Реакции с участием аминогруппы -аминокислот Реакции дезаминирования. окислительное дезаминирование СН 3 –СН–СООН [O] NH 2 СН 3 –С – СООH + NH 3 пировиноградная O кислота восстановительное дезаминирование СН 3 –СН–СООН [Н] NH 2 СН 3 –СН 2 – СООH пропановая кислота + NH 3 гидролитическое дезаминирование СН 3 –СН–СООН NH 2 Н 2 О СН 3 –СН–СООH молочная HО кислота + NH 3 внутримолекулярное дезаминирование СН 3 –СН–СООН NH 2 СН 2 = СН – СООH пропеновая кислота + NH 3 Реакция трансаминирования. СН 3 –СН–СООН NH 2 НООС–СН 2–С – СООH + кетоглутаровая кислота O СН 3 –С–СООН O НООС–СН 2–СН– СООH NH 2
Реакции с участием аминогруппы -аминокислот Реакции дезаминирования. окислительное дезаминирование СН 3 –СН–СООН [O] NH 2 СН 3 –С – СООH + NH 3 пировиноградная O кислота восстановительное дезаминирование СН 3 –СН–СООН [Н] NH 2 СН 3 –СН 2 – СООH пропановая кислота + NH 3 гидролитическое дезаминирование СН 3 –СН–СООН NH 2 Н 2 О СН 3 –СН–СООH молочная HО кислота + NH 3 внутримолекулярное дезаминирование СН 3 –СН–СООН NH 2 СН 2 = СН – СООH пропеновая кислота + NH 3 Реакция трансаминирования. СН 3 –СН–СООН NH 2 НООС–СН 2–С – СООH + кетоглутаровая кислота O СН 3 –С–СООН O НООС–СН 2–СН– СООH NH 2
 Образование пептидной связи Амино и карбоксильные группы аминокислот могут реагировать друг с другом и без образования цикла: H 2 N –СН–СООН + H 2 N –СН–СООН СН 3 СН 2 ОН H 2 N –СН–СО–NН –СН–СООН –H 2 O СН 3 СН 2 ОН дипептид аланин серин аланилсерин Возникающая при этом связь –СО–NН– называется пептидной связью, а продукт взаимодействия аминокислот – пептидом. Если в реакцию вступили 2 аминокислоты, получается дипептид; 3 аминокислоты – трипептид и т. д. Пептиды молекулярной массой не более 10 000 называют олигопептидами, молекулярной массой более 10 000 – полипептидами, или белками. Пептидные связи в составе пептидов по химической природе являются амидными. Полипептидная цепь состоит из регулярно повторяющихся участков, образующих остов молекулы, и вариабельных участков – боковых радикалов аминокислотных остатков. Началом полипептидной цепи считают конец, несущий свободную аминогруппу (N конец), а заканчивается полипептидная цепь свободной карбоксильной группой (С конец). Называют пептид, последовательно перечисляя, начиная с N конца, названия аминокислот, входящих в пептид; при этом суффикс «ин» заменяют на суффикс «ил» для всех аминокислот, кроме С концевой. Для описания строения пептидов применяют не традиционные структурные формулы, а сокращенные обозначения, позволяющие сделать запись более компактной. H 2 N –СН–СОNН –СН–СОNH –СН 2–СОNН –СН–СОOH СН 2 SH СН 3 CH(СН 3)2 СН 2 ОН Пентапептид: цистеилаланилглицилвалилсерин или Цис–Ала–Гли–Вал–Сер
Образование пептидной связи Амино и карбоксильные группы аминокислот могут реагировать друг с другом и без образования цикла: H 2 N –СН–СООН + H 2 N –СН–СООН СН 3 СН 2 ОН H 2 N –СН–СО–NН –СН–СООН –H 2 O СН 3 СН 2 ОН дипептид аланин серин аланилсерин Возникающая при этом связь –СО–NН– называется пептидной связью, а продукт взаимодействия аминокислот – пептидом. Если в реакцию вступили 2 аминокислоты, получается дипептид; 3 аминокислоты – трипептид и т. д. Пептиды молекулярной массой не более 10 000 называют олигопептидами, молекулярной массой более 10 000 – полипептидами, или белками. Пептидные связи в составе пептидов по химической природе являются амидными. Полипептидная цепь состоит из регулярно повторяющихся участков, образующих остов молекулы, и вариабельных участков – боковых радикалов аминокислотных остатков. Началом полипептидной цепи считают конец, несущий свободную аминогруппу (N конец), а заканчивается полипептидная цепь свободной карбоксильной группой (С конец). Называют пептид, последовательно перечисляя, начиная с N конца, названия аминокислот, входящих в пептид; при этом суффикс «ин» заменяют на суффикс «ил» для всех аминокислот, кроме С концевой. Для описания строения пептидов применяют не традиционные структурные формулы, а сокращенные обозначения, позволяющие сделать запись более компактной. H 2 N –СН–СОNН –СН–СОNH –СН 2–СОNН –СН–СОOH СН 2 SH СН 3 CH(СН 3)2 СН 2 ОН Пентапептид: цистеилаланилглицилвалилсерин или Цис–Ала–Гли–Вал–Сер
 Белки В настоящее время общепризнанной является полипептидная теория строения белковой молекулы. Белки можно классифицировать: – по форме молекул (глобулярные и фибриллярные); – по молекулярной массе (низко и высокомолекулярные); – по составу или химическому строению (простые и сложные); – по выполняемым функциям; – по локализации в клетке (ядерные, цитоплазматические и др.); – по локализации в организме (белки крови, печени и др.); – по возможности адаптивно регулировать количество данных белков: белки, синтезирующиеся с постоянной скоростью (конститутивные), и белки, синтез которых может усиливаться при воздействии факторов среды (индуцибельные); – по продолжительности жизни в клетке (от очень быстро обновляющихся белков, с периодом полупревращения менее 1 ч, до очень медленно обновляющихся белков, период полупревращения которых исчисляют неделями и месяцами); – по схожим участкам первичной структуры и родственным функциям (семейства белков).
Белки В настоящее время общепризнанной является полипептидная теория строения белковой молекулы. Белки можно классифицировать: – по форме молекул (глобулярные и фибриллярные); – по молекулярной массе (низко и высокомолекулярные); – по составу или химическому строению (простые и сложные); – по выполняемым функциям; – по локализации в клетке (ядерные, цитоплазматические и др.); – по локализации в организме (белки крови, печени и др.); – по возможности адаптивно регулировать количество данных белков: белки, синтезирующиеся с постоянной скоростью (конститутивные), и белки, синтез которых может усиливаться при воздействии факторов среды (индуцибельные); – по продолжительности жизни в клетке (от очень быстро обновляющихся белков, с периодом полупревращения менее 1 ч, до очень медленно обновляющихся белков, период полупревращения которых исчисляют неделями и месяцами); – по схожим участкам первичной структуры и родственным функциям (семейства белков).
 Функции белков Функция белка Каталитическая (ферментативная) Транспортная Структурная (пластическая) Сократительная Регуляторная (гормональная) Защитная Энергетическая Сущность Примеры Ускорение химических реакций Пепсин, трипсин, в организме каталаза, цитохромоксидаза Транспорт (перенос) Гемоглобин, альбумин, химических соединений в трансферрин организме Обеспечение прочности и Коллаген, эластичности тканей кератин Укорочение саркомеров мышцы Актин, миозин (сокращение) Регуляция обмена веществ в инсулин, соматотропин, клетках и тканях глюкагон, кортикотрспин Защита организма от Интерфероны, повреждающих факторов иммуноглобулины, фибриноген, тромбин Высвобождение энергии за счёт Белки пищи и тканей распада аминокислот
Функции белков Функция белка Каталитическая (ферментативная) Транспортная Структурная (пластическая) Сократительная Регуляторная (гормональная) Защитная Энергетическая Сущность Примеры Ускорение химических реакций Пепсин, трипсин, в организме каталаза, цитохромоксидаза Транспорт (перенос) Гемоглобин, альбумин, химических соединений в трансферрин организме Обеспечение прочности и Коллаген, эластичности тканей кератин Укорочение саркомеров мышцы Актин, миозин (сокращение) Регуляция обмена веществ в инсулин, соматотропин, клетках и тканях глюкагон, кортикотрспин Защита организма от Интерфероны, повреждающих факторов иммуноглобулины, фибриноген, тромбин Высвобождение энергии за счёт Белки пищи и тканей распада аминокислот
 Классификация простых белков Альбумины. Примерно 75 80% осмотического давления белков сыворотки крови приходится на альбумины; еще одна функция – транспорт жирных кислот. Глобулины содержатся в крови в комплексе с билирубином и с липопротеинами высокой плотности. Фракция β глобулинов включает протромбин, являющийся предшественником тромбина белка, ответственного за превращение фибриногена крови в фибрин при свертывании крови. Глобулины выполняют защитную функцию. Протамины – низкомолекулярные белки, обладающие выраженными основными свойствами, обусловленными наличием в их составе от 60 до 85% аргинина. В ядрах клеток ассоциируются с ДНК. Гистоны также являются небольшими белками основного характера. В их состав входят лизин и аргинин (20 30%). Гистоны играют важную роль в регуляции экспрессии генов. Проламины белки растительного происхождения, содержатся в основном в семенах злаков. Все белки этой группы при гидролизе дают значительное количество пролина. Проламины содержат 20 25% глутаминовой кислоты и 10 15% пролина. Наиболее изучены оризенин (из риса), глютенин (из пшеницы), зеин (из кукурузы), и др. Глютелины простые белки, содержатся в семенах злаков, в зелёных частях растений. Для глютелинов характерно сравнительно высокое содержание глутаминовой кислоты и наличие лизина. Глютелины – запасные белки.
Классификация простых белков Альбумины. Примерно 75 80% осмотического давления белков сыворотки крови приходится на альбумины; еще одна функция – транспорт жирных кислот. Глобулины содержатся в крови в комплексе с билирубином и с липопротеинами высокой плотности. Фракция β глобулинов включает протромбин, являющийся предшественником тромбина белка, ответственного за превращение фибриногена крови в фибрин при свертывании крови. Глобулины выполняют защитную функцию. Протамины – низкомолекулярные белки, обладающие выраженными основными свойствами, обусловленными наличием в их составе от 60 до 85% аргинина. В ядрах клеток ассоциируются с ДНК. Гистоны также являются небольшими белками основного характера. В их состав входят лизин и аргинин (20 30%). Гистоны играют важную роль в регуляции экспрессии генов. Проламины белки растительного происхождения, содержатся в основном в семенах злаков. Все белки этой группы при гидролизе дают значительное количество пролина. Проламины содержат 20 25% глутаминовой кислоты и 10 15% пролина. Наиболее изучены оризенин (из риса), глютенин (из пшеницы), зеин (из кукурузы), и др. Глютелины простые белки, содержатся в семенах злаков, в зелёных частях растений. Для глютелинов характерно сравнительно высокое содержание глутаминовой кислоты и наличие лизина. Глютелины – запасные белки.
 Классификация сложных белков Название класса Нуклеопротеины Простетическая группа Окрашенные соединения (гемопротеины, флавопротеины) Нуклеиновые кислоты Фосфопротеины Фосфорная кислота Хромопротеины Металлопротеины Ионы металлов Гликопротеины Липопротеины Углеводы и их производные Липиды и их производные Представители класса Гемоглобин, миоглобин, цитохромы, каталаза, пероксидаза Вирусы, рибосомы, хроматин Казеин молока, овальбумин, вителлин, ихтулин Ферритин, трансферрин, церулоплазмин, гемосидерин Гликофорин, интерферон, иммуноглобулины, муцин Хиломикроны, липопротеины плазмы крови, липовителин
Классификация сложных белков Название класса Нуклеопротеины Простетическая группа Окрашенные соединения (гемопротеины, флавопротеины) Нуклеиновые кислоты Фосфопротеины Фосфорная кислота Хромопротеины Металлопротеины Ионы металлов Гликопротеины Липопротеины Углеводы и их производные Липиды и их производные Представители класса Гемоглобин, миоглобин, цитохромы, каталаза, пероксидаза Вирусы, рибосомы, хроматин Казеин молока, овальбумин, вителлин, ихтулин Ферритин, трансферрин, церулоплазмин, гемосидерин Гликофорин, интерферон, иммуноглобулины, муцин Хиломикроны, липопротеины плазмы крови, липовителин
 Первичная структура белка Первичная структура белка – это последовательность расположения аминокислот в полипептидной цепи. Её определяют, последовательно отщепляя аминокислоты от белка путём гидролиза. Для отщепления N концевой аминокислоты белок обрабатывают 2, 4 динитрофторбензолом и после кислотного гидролиза только одна N концевая кислота оказывается связанной с этим реактивом (метод Сэнджера). По методу Эдмана в процессе гидролиза отделяют N концевую кислоту в виде продукта взаимодействия с фенилизотиоцианатом. Для определения С концевой кислоты обычно используют гидролиз в присутствии специального фермента – карбоксипептидазы, которая разрывает пептидную связь с того конца пептида, где содержится свободная карбоксильная группа. Существуют и химические методы отщепления С концевой кислоты, например с использованием гидразина (метод Акабори).
Первичная структура белка Первичная структура белка – это последовательность расположения аминокислот в полипептидной цепи. Её определяют, последовательно отщепляя аминокислоты от белка путём гидролиза. Для отщепления N концевой аминокислоты белок обрабатывают 2, 4 динитрофторбензолом и после кислотного гидролиза только одна N концевая кислота оказывается связанной с этим реактивом (метод Сэнджера). По методу Эдмана в процессе гидролиза отделяют N концевую кислоту в виде продукта взаимодействия с фенилизотиоцианатом. Для определения С концевой кислоты обычно используют гидролиз в присутствии специального фермента – карбоксипептидазы, которая разрывает пептидную связь с того конца пептида, где содержится свободная карбоксильная группа. Существуют и химические методы отщепления С концевой кислоты, например с использованием гидразина (метод Акабори).
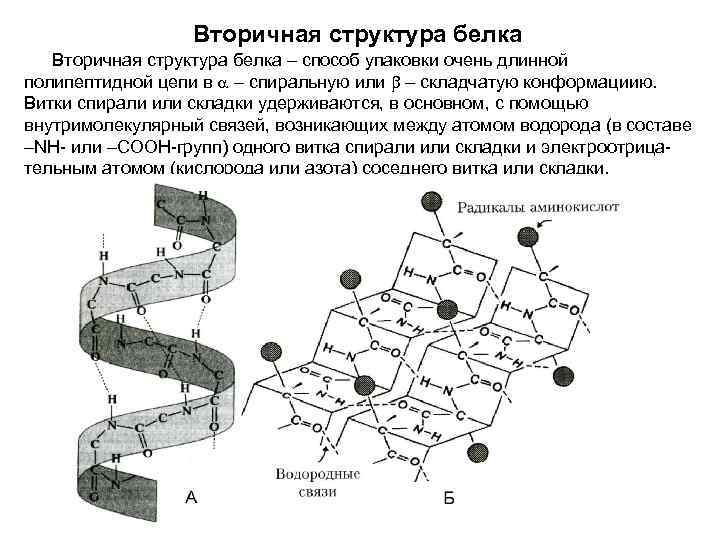 Вторичная структура белка – способ упаковки очень длинной полипептидной цепи в – спиральную или – складчатую конформациию. Витки спирали или складки удерживаются, в основном, с помощью внутримолекулярный связей, возникающих между атомом водорода (в составе –NН или –СООН групп) одного витка спирали или складки и электроотрица тельным атомом (кислорода или азота) соседнего витка или складки.
Вторичная структура белка – способ упаковки очень длинной полипептидной цепи в – спиральную или – складчатую конформациию. Витки спирали или складки удерживаются, в основном, с помощью внутримолекулярный связей, возникающих между атомом водорода (в составе –NН или –СООН групп) одного витка спирали или складки и электроотрица тельным атомом (кислорода или азота) соседнего витка или складки.
 Третичная структура белка Третичная структура белка – трёхмерная пространственная ориентация полипептидной спирали или складчатой структуры в определённом объёме. Различают глобулярную (шарообразную) и фибриллярную (вытянутую, волокнистую) третичную структуры. Третичная структура формируется автоматически, самопроизвольно и полностью определяется первичной структурой белка. При этом во взаимодействие вступают боковые радикалы аминокислотных остатков. Стабилизация третичной структуры осуществляется за счёт образования между радикалами аминокислот водородных, ионных, дисульфидных связей, а также благодаря ван дер ваальсовым силам притяжения между неполярными углеводородными радикалами.
Третичная структура белка Третичная структура белка – трёхмерная пространственная ориентация полипептидной спирали или складчатой структуры в определённом объёме. Различают глобулярную (шарообразную) и фибриллярную (вытянутую, волокнистую) третичную структуры. Третичная структура формируется автоматически, самопроизвольно и полностью определяется первичной структурой белка. При этом во взаимодействие вступают боковые радикалы аминокислотных остатков. Стабилизация третичной структуры осуществляется за счёт образования между радикалами аминокислот водородных, ионных, дисульфидных связей, а также благодаря ван дер ваальсовым силам притяжения между неполярными углеводородными радикалами.
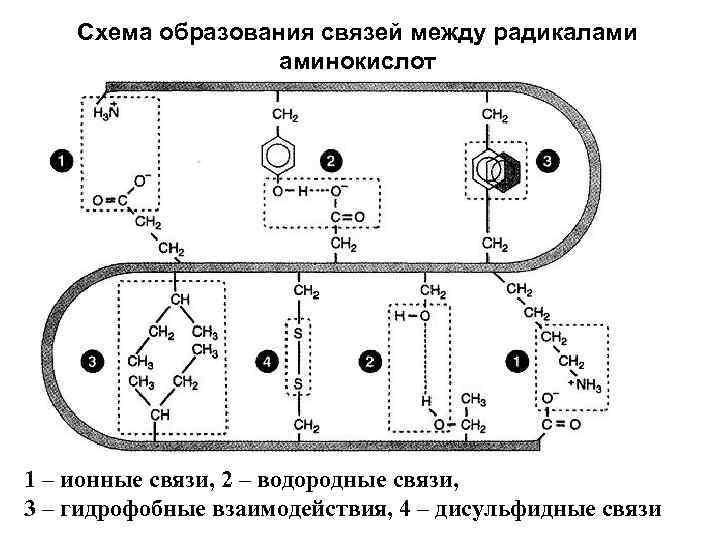 Схема образования связей между радикалами аминокислот 1 – ионные связи, 2 – водородные связи, 3 – гидрофобные взаимодействия, 4 – дисульфидные связи
Схема образования связей между радикалами аминокислот 1 – ионные связи, 2 – водородные связи, 3 – гидрофобные взаимодействия, 4 – дисульфидные связи
 Четвертичная структура белка Четвертичная структура белка – способ укладки в пространстве отдельных полипептидных цепей и формирование структурно и функционально единого макромолекулярного образования. Образовавшуюся молекулу называют олигомером, а отдельные полипептидные цепи, из которых он состоит – протомерами, мономерами или субъединицами (их обычно чётное количество: 2, 4, реже 6 или 8). Например, молекула гемоглобина состоит из двух – и двух – полипептидных цепей. Каждая полипептидная цепь окружает группу гема – небелкового пигмента, придающего крови её красный цвет. Именно в составе гема находится катион железа, способный присоединять и транспортировать по организму необходимый для функционирования организма кислород. Тетрамер гемоглобина Четвертичной структурой обладает около 5% белков, в том числе гемоглобин, иммуно глобулины, инсулин, ферритин, почти все ДНК и РНК полимеразы. Гексамер инсулина
Четвертичная структура белка Четвертичная структура белка – способ укладки в пространстве отдельных полипептидных цепей и формирование структурно и функционально единого макромолекулярного образования. Образовавшуюся молекулу называют олигомером, а отдельные полипептидные цепи, из которых он состоит – протомерами, мономерами или субъединицами (их обычно чётное количество: 2, 4, реже 6 или 8). Например, молекула гемоглобина состоит из двух – и двух – полипептидных цепей. Каждая полипептидная цепь окружает группу гема – небелкового пигмента, придающего крови её красный цвет. Именно в составе гема находится катион железа, способный присоединять и транспортировать по организму необходимый для функционирования организма кислород. Тетрамер гемоглобина Четвертичной структурой обладает около 5% белков, в том числе гемоглобин, иммуно глобулины, инсулин, ферритин, почти все ДНК и РНК полимеразы. Гексамер инсулина
 Цветные реакции для обнаружения белков и аминокислот Для идентификации пептидов, белков и отдельных аминокислот используют так называемые «цветные реакции» . Универсальная реакция на пептидную группу – появление красно фиолетовой окраски при добавлении к раствору белка ионов меди (II) в щелочной среде (биуретовая реакция). Реакция на остатки ароматических аминокислот – тирозина и фенилаланина – появление желтой окраски при обработке раствора белка концентрированной азотной кислотой (ксантопротеиновая реакция). Серусодержащие белки дают черное окрашивание при нагревании с раствором ацетата свинца(II) в щелочной среде (реакция Фоля). Общая качественная реакция аминокислот - образование сине фиолетового окрашивания при взаимодействии с нингидрином. Нингидриновую реакцию дают также и белки.
Цветные реакции для обнаружения белков и аминокислот Для идентификации пептидов, белков и отдельных аминокислот используют так называемые «цветные реакции» . Универсальная реакция на пептидную группу – появление красно фиолетовой окраски при добавлении к раствору белка ионов меди (II) в щелочной среде (биуретовая реакция). Реакция на остатки ароматических аминокислот – тирозина и фенилаланина – появление желтой окраски при обработке раствора белка концентрированной азотной кислотой (ксантопротеиновая реакция). Серусодержащие белки дают черное окрашивание при нагревании с раствором ацетата свинца(II) в щелочной среде (реакция Фоля). Общая качественная реакция аминокислот - образование сине фиолетового окрашивания при взаимодействии с нингидрином. Нингидриновую реакцию дают также и белки.
 Значение белков и пептидов Белки составляют материальную основу химической деятельности клетки. Функции белков в природе универсальны. Среди них различают ферменты, гормоны, структурные (кератин, фиброин, коллаген), транспортные (гемоглобин, миоглобин), двигательные (актин, миозин), защитные (иммуноглобулины), запасные (казеин, яичный альбумин) белки, токсины (змеиные яды, дифтерийный токсин). В биологическом плане пептиды отличаются от белков более узким спектром функций. Наиболее характерна для пептидов регуляторная функция (гормоны, антибиотики, токсины, ингибиторы и активаторы ферментов, переносчики ионов через мембраны и т. д.). Недавно открыта группа пептидов головного мозга - нейропептидов. Они влияют на процессы обучения и запоминания, регулируют сон, обладают обезболивающей функцией; прослеживается связь некоторых нервно психических заболеваний например шизофрении, с содержанием тех или иных пептидов в мозге. В настоящее время достигнуты успехи в изучении проблемы соотношения структуры и функций белков, механизма их участия в важнейших процессах жизнедеятельности организма, понимании молекулярных основ патогенеза многих болезней. К числу актуальных проблем относится химический синтез белка. Получение синтетическим путем аналогов природных пептидов и белков призвано способствовать решению таких вопросов, как выяснение механизма действия этих соединений в клетке, установление взаимосвязи их активности с пространственным строением, создание новых лекарственных средств и продуктов питания, а также позволяет подойти к моделированию процессов, протекающих в организме.
Значение белков и пептидов Белки составляют материальную основу химической деятельности клетки. Функции белков в природе универсальны. Среди них различают ферменты, гормоны, структурные (кератин, фиброин, коллаген), транспортные (гемоглобин, миоглобин), двигательные (актин, миозин), защитные (иммуноглобулины), запасные (казеин, яичный альбумин) белки, токсины (змеиные яды, дифтерийный токсин). В биологическом плане пептиды отличаются от белков более узким спектром функций. Наиболее характерна для пептидов регуляторная функция (гормоны, антибиотики, токсины, ингибиторы и активаторы ферментов, переносчики ионов через мембраны и т. д.). Недавно открыта группа пептидов головного мозга - нейропептидов. Они влияют на процессы обучения и запоминания, регулируют сон, обладают обезболивающей функцией; прослеживается связь некоторых нервно психических заболеваний например шизофрении, с содержанием тех или иных пептидов в мозге. В настоящее время достигнуты успехи в изучении проблемы соотношения структуры и функций белков, механизма их участия в важнейших процессах жизнедеятельности организма, понимании молекулярных основ патогенеза многих болезней. К числу актуальных проблем относится химический синтез белка. Получение синтетическим путем аналогов природных пептидов и белков призвано способствовать решению таких вопросов, как выяснение механизма действия этих соединений в клетке, установление взаимосвязи их активности с пространственным строением, создание новых лекарственных средств и продуктов питания, а также позволяет подойти к моделированию процессов, протекающих в организме.
 Кое-что интересное о белках Белки являются основой разного рода биологических клеев. Так, ловчие сети пауков состоят в основном из фиброина – белка, выделяемого паутинными бородавками. Это сиропообразное вязкое вещество затвердевает на воздухе, превращаясь в прочную и нерастворимую в воде нить. Шелковинки, образующие спиральную нить паутины, содержат клей, удерживающий добычу. Сам паук свободно бегает по радиальным нитям. Благодаря специальным клеям мухи и др. насекомые способны проявлять просто чудеса акробатики. Бабочки приклеивают к листьям растений свои яйца, некоторые виды стрижей строят гнезда из застывающих выделений слюнных желез, осетровые крепят икру на придонных камнях. Некоторые виды улиток на зиму или в периоды засухи снабжают раковины специальной «дверью» , которую сама улитка возводит из клейкого твердеющего протеина, содержащего известь. Отгородившись от внешнего мира достаточно твердой преградой, улитка пережидает неблагоприятные времена в раковине. Когда ситуация меняется, она просто съедает ее и перестает жить затворницей. Клеящие вещества, которыми пользуются подводные жители, должны застывать под водой. Поэтому в их состав входят несколько различных протеинов, отталкивающих воду и взаимодействующих между собой с образованием прочного клея. Клей, которым мидии прикрепляются к камню, не растворяется в воде и вдвое крепче эпоксидной смолы. Сейчас этот протеин пытаются синтезировать в лабораторных условиях. Большинство клеящих веществ не переносят влаги, а белковым клеем мидий можно было бы склеивать кости и зубы. Этот белок не вызывает отторжения организмом, что очень важно для медицинских препаратов.
Кое-что интересное о белках Белки являются основой разного рода биологических клеев. Так, ловчие сети пауков состоят в основном из фиброина – белка, выделяемого паутинными бородавками. Это сиропообразное вязкое вещество затвердевает на воздухе, превращаясь в прочную и нерастворимую в воде нить. Шелковинки, образующие спиральную нить паутины, содержат клей, удерживающий добычу. Сам паук свободно бегает по радиальным нитям. Благодаря специальным клеям мухи и др. насекомые способны проявлять просто чудеса акробатики. Бабочки приклеивают к листьям растений свои яйца, некоторые виды стрижей строят гнезда из застывающих выделений слюнных желез, осетровые крепят икру на придонных камнях. Некоторые виды улиток на зиму или в периоды засухи снабжают раковины специальной «дверью» , которую сама улитка возводит из клейкого твердеющего протеина, содержащего известь. Отгородившись от внешнего мира достаточно твердой преградой, улитка пережидает неблагоприятные времена в раковине. Когда ситуация меняется, она просто съедает ее и перестает жить затворницей. Клеящие вещества, которыми пользуются подводные жители, должны застывать под водой. Поэтому в их состав входят несколько различных протеинов, отталкивающих воду и взаимодействующих между собой с образованием прочного клея. Клей, которым мидии прикрепляются к камню, не растворяется в воде и вдвое крепче эпоксидной смолы. Сейчас этот протеин пытаются синтезировать в лабораторных условиях. Большинство клеящих веществ не переносят влаги, а белковым клеем мидий можно было бы склеивать кости и зубы. Этот белок не вызывает отторжения организмом, что очень важно для медицинских препаратов.
 Кое-что интересное о белках У метилового эфира L аспартил L фенилаланина очень сладкий вкус. СН 3 ООС-СН(СН 2 С 6 Н 5)-NH-СО- СH(NН 2)-СН 2-СООН. Вещество известно под торговым названием «аспартам» . Аспартам не только слаще сахара (в 100- 150 раз), но и усиливает его сладкий вкус, особенно в присутствии лимонной кислоты. Сладки и многие из производных аcпартама. Из ягод Dioscoreophylum cumminsii (русского названия нет), найденных в дебрях Нигерии в 1895 году, выделен белок монелин, который слаще сахара в 1500 - 2000 раз. Еще сильнее - в 4000 раз - превзошел сахарозу белок тауматин, выделенный из ярко красных мясистых плодов другого африканского растения Thaumatococcus daniellii. Интенсивность сладкого вкуса тауматина еще больше увеличивается при взаимодействии этого белка с ионами алюминия. Образующийся комплекс, получивший торговое название талин, слаще сахарозы в 35 000 раз; если же сравнивать не массы талина и сахарозы, а число их молекул, то талин окажется слаще уже в 200 тысяч раз! Еще один очень сладкий белок - миракулин был выделен в прошлом веке из красных плодов кустарника Synsepalum dulcificum daniellii, которые назвали «чудодейственными»: у пожевавшего эти плоды человека изменяются вкусовые ощущения. Так, у уксуса, появляется приятный винный вкус, лимонный сок превращается в сладкий напиток, причем эффект продолжается длительное время. Если когда нибудь будут выращивать на плантациях все эти экзотические плоды, у сахарной промышленности будет куда меньше проблем с транспортировкой продукции. Ведь маленький кусочек тауматина сможет заменить целый мешок сахарного песка! В начале 70 х годов было синтезировано соединение, самое сладкое из всех синтезированных. Это дипептид, построенный из остатков двух аминокислот - аспарагиновой и аминомалоновой. В дипептиде две карбоксильные группы остатка аминомалоновой кислоты заменены на сложноэфирные группы, образованные метанолом и фенхолом (он содержится в эфирных маслах растений и добывается из скипидара). Это вещество в примерно в 33 000 раз слаще сахарозы. Чтобы плитка шоколада стала привычно сладкой, достаточно долей миллиграмма этой специи.
Кое-что интересное о белках У метилового эфира L аспартил L фенилаланина очень сладкий вкус. СН 3 ООС-СН(СН 2 С 6 Н 5)-NH-СО- СH(NН 2)-СН 2-СООН. Вещество известно под торговым названием «аспартам» . Аспартам не только слаще сахара (в 100- 150 раз), но и усиливает его сладкий вкус, особенно в присутствии лимонной кислоты. Сладки и многие из производных аcпартама. Из ягод Dioscoreophylum cumminsii (русского названия нет), найденных в дебрях Нигерии в 1895 году, выделен белок монелин, который слаще сахара в 1500 - 2000 раз. Еще сильнее - в 4000 раз - превзошел сахарозу белок тауматин, выделенный из ярко красных мясистых плодов другого африканского растения Thaumatococcus daniellii. Интенсивность сладкого вкуса тауматина еще больше увеличивается при взаимодействии этого белка с ионами алюминия. Образующийся комплекс, получивший торговое название талин, слаще сахарозы в 35 000 раз; если же сравнивать не массы талина и сахарозы, а число их молекул, то талин окажется слаще уже в 200 тысяч раз! Еще один очень сладкий белок - миракулин был выделен в прошлом веке из красных плодов кустарника Synsepalum dulcificum daniellii, которые назвали «чудодейственными»: у пожевавшего эти плоды человека изменяются вкусовые ощущения. Так, у уксуса, появляется приятный винный вкус, лимонный сок превращается в сладкий напиток, причем эффект продолжается длительное время. Если когда нибудь будут выращивать на плантациях все эти экзотические плоды, у сахарной промышленности будет куда меньше проблем с транспортировкой продукции. Ведь маленький кусочек тауматина сможет заменить целый мешок сахарного песка! В начале 70 х годов было синтезировано соединение, самое сладкое из всех синтезированных. Это дипептид, построенный из остатков двух аминокислот - аспарагиновой и аминомалоновой. В дипептиде две карбоксильные группы остатка аминомалоновой кислоты заменены на сложноэфирные группы, образованные метанолом и фенхолом (он содержится в эфирных маслах растений и добывается из скипидара). Это вещество в примерно в 33 000 раз слаще сахарозы. Чтобы плитка шоколада стала привычно сладкой, достаточно долей миллиграмма этой специи.
 Кое-что интересное о белках Химические и физические свойства кожи и волос определяются свойствами кератинов. У каждого вида животных кератин имеет некоторые особенности, поэтому это слово употребляют во множественном числе. КЕРАТИНЫ - нерастворимые в воде белки позвоночных, образующие их волосы, шерсть, роговой слой кожи, ногти. Под действием воды кератин кожи, волос, ногтей размягчается, разбухает, а после испарения воды снова затвердевает. Основная химическая особенность кератина заключается в том, что в его составе до 15% содержащей серу аминокислоты цистеина. Атомы серы, присутствующие в цистеиновой части молекулы кератина, легко образуют связи с атомами серы соседней молекулы, возникают дисульфидные мостики, которые соединяют эти макромолекулы. Кератины относятся к фибриллярным белкам. В тканях они существуют в виде длинных нитей - фибрилл, в которых молекулы расположены пучками, направленными в одну сторону. В этих нитях отдельные макромолекулы соединены между собой также химическими связями (рис. 1). Спиральные нити закручены в тройную спираль, а 11 спиралей объединены в микрофибриллу, которая составляет центральную часть волоса (см. рис. 2). Микрофибриллы объединяются в макрофибриллы. а) Водородные б) Ионные в) Неполярные г) Дисульфид Рис. 2. Кератин волос - фибриллярный белок. связи связи взаимодействия ный мостик Рис. 1. Типы взаимодействия между цепочечными белковыми молекулами
Кое-что интересное о белках Химические и физические свойства кожи и волос определяются свойствами кератинов. У каждого вида животных кератин имеет некоторые особенности, поэтому это слово употребляют во множественном числе. КЕРАТИНЫ - нерастворимые в воде белки позвоночных, образующие их волосы, шерсть, роговой слой кожи, ногти. Под действием воды кератин кожи, волос, ногтей размягчается, разбухает, а после испарения воды снова затвердевает. Основная химическая особенность кератина заключается в том, что в его составе до 15% содержащей серу аминокислоты цистеина. Атомы серы, присутствующие в цистеиновой части молекулы кератина, легко образуют связи с атомами серы соседней молекулы, возникают дисульфидные мостики, которые соединяют эти макромолекулы. Кератины относятся к фибриллярным белкам. В тканях они существуют в виде длинных нитей - фибрилл, в которых молекулы расположены пучками, направленными в одну сторону. В этих нитях отдельные макромолекулы соединены между собой также химическими связями (рис. 1). Спиральные нити закручены в тройную спираль, а 11 спиралей объединены в микрофибриллу, которая составляет центральную часть волоса (см. рис. 2). Микрофибриллы объединяются в макрофибриллы. а) Водородные б) Ионные в) Неполярные г) Дисульфид Рис. 2. Кератин волос - фибриллярный белок. связи связи взаимодействия ный мостик Рис. 1. Типы взаимодействия между цепочечными белковыми молекулами
 Кое-что интересное о белках Волос имеет неоднородную структуру в поперечном сечении. С точки зрения химии все слои волоса идентичны и состоят из одного химического соединения - кератина. Но в зависи мости от степени и типа структурирования кератина существуют слои с различными свойствами: кутикула - поверхностный чешуйчатый слой; волокнистый, или корковый, слой; сердцевина. Кутикула образуется из плоских клеток, перекрывающих друга подобно рыбьей чешуе. С точки зрения косметики это наиболее важный слой волоса. Именно от его состояния зависит внешний вид волос: блеск, упругость или, наоборот, тусклость, посеченность. Состояние кутикулы влияет и на процессы окраски волос и их завивки, так как для проникновения препаратов в более глубокие слои волоса, к пигменту, необходимо размягчить кутикулу. Кератин, из которого состоят «чешуйки» , разбухает под действием влаги, особенно если это сопровождается действием тепла и щелочных препаратов (мыло). С точки зрения химии это объясняется разрывом водородных связей в молекулах кератина, которые при высыхании волос восстанавливаются. При набухании пластинок их края встают вертикально, волос теряет блеск. Размягчение кутикулы уменьшает и механическую прочность волоса: во влажном состоянии его легче повредить. Пространство между краями чешуек заполнено кожным жиром, что придает волосам блеск, мягкость, эластичность. Волокнистый, или корковый, слой образован длинными веретенообразными ороговевшими клетками, расположенными в одном направлении; от него зависят эластичность и упругость волоса. В этом слое содержится пигмент меланин, «ответственный» за цвет волос. Окраска волоса зависит от присутствия в нем меланина и пузырьков воздуха. Светлые волосы содержат рассеянный пигмент, темные - зернистый. Сердцевина, или мозговой слой, состоит из не полностью ороговевших клеток.
Кое-что интересное о белках Волос имеет неоднородную структуру в поперечном сечении. С точки зрения химии все слои волоса идентичны и состоят из одного химического соединения - кератина. Но в зависи мости от степени и типа структурирования кератина существуют слои с различными свойствами: кутикула - поверхностный чешуйчатый слой; волокнистый, или корковый, слой; сердцевина. Кутикула образуется из плоских клеток, перекрывающих друга подобно рыбьей чешуе. С точки зрения косметики это наиболее важный слой волоса. Именно от его состояния зависит внешний вид волос: блеск, упругость или, наоборот, тусклость, посеченность. Состояние кутикулы влияет и на процессы окраски волос и их завивки, так как для проникновения препаратов в более глубокие слои волоса, к пигменту, необходимо размягчить кутикулу. Кератин, из которого состоят «чешуйки» , разбухает под действием влаги, особенно если это сопровождается действием тепла и щелочных препаратов (мыло). С точки зрения химии это объясняется разрывом водородных связей в молекулах кератина, которые при высыхании волос восстанавливаются. При набухании пластинок их края встают вертикально, волос теряет блеск. Размягчение кутикулы уменьшает и механическую прочность волоса: во влажном состоянии его легче повредить. Пространство между краями чешуек заполнено кожным жиром, что придает волосам блеск, мягкость, эластичность. Волокнистый, или корковый, слой образован длинными веретенообразными ороговевшими клетками, расположенными в одном направлении; от него зависят эластичность и упругость волоса. В этом слое содержится пигмент меланин, «ответственный» за цвет волос. Окраска волоса зависит от присутствия в нем меланина и пузырьков воздуха. Светлые волосы содержат рассеянный пигмент, темные - зернистый. Сердцевина, или мозговой слой, состоит из не полностью ороговевших клеток.
Среди органических веществ белки , или протеины , - самые многочисленные, наиболее разнообразные и имеющие первостепенное значение биополимеры. На их долю приходится 50 - 80% сухой массы клетки.
Молекулы белков имеют большие размеры, поэтому их называют макромолекулами . Кроме углерода , кислорода , водорода и азота , в состав белков могут входить сера, фосфор и железо. Белки отличаются друг от друга числом (от ста до нескольких тысяч), составом и последовательностью мономеров. Мономерами белков являются аминокислоты (рис. 1)
Бесконечное разнообразие белков создается за счет различного сочетания всего 20 аминокислот. Каждая аминокислота имеет свое название, особое строение и свойства. Их общую формулу можно представить в следующем виде:
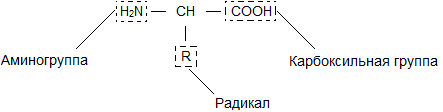
Молекула аминокислоты состоит из двух одинаковых для всех аминокислот частей, одна из которых является аминогруппой (-NH 2 ) с основными свойствами, другая - карбоксильной группой (-COOH ) с кислотными свойствами. Часть молекулы, называемая радикалом (R ), у разных аминокислот имеет различное строение. Наличие в одной молекуле аминокислоты основной и кислотной групп обусловливает их высокую реакционную способность. через эти группы происходит соединение аминокислот при образовании белка. При этом возникает молекула воды, а освободившиеся электроны образуют пептидную связь. Поэтому белки называют полипептидами .
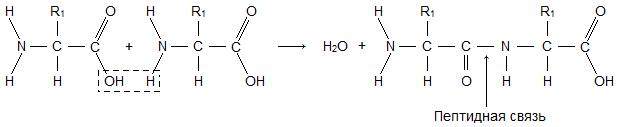
Молекулы белков могут иметь различные пространственные конфигурации, и в их строении различают четыре уровня структурной организации.
Последовательность аминокислот в составе полипептидной цепи представляет первичную структуру
белка. Она уникальна для любого белка и определяет его форму, свойства и функции.
Большинство белков имеют вид спирали в результате образования водородных связей между -CO-
и -NH-
группами разных аминокислотных остатков полипептидной цепи. Водородные связи малопрочные, но в комплексе они обеспечивают довольно прочную структуру. Эта спираль - вторичная структура
белка.
Третичная структура - трехмерная пространственная «упаковка» полипептидной цепи. В результате возникает причудливая, но для каждого белка специфическая конфигурация - глобула . Прочность третичной структуры обеспечивается разнообразными связями, возникающими между радикалами аминокислот.
Четвертичная структура
характерна не для всех белков. Она возникает в результате соединения нескольких макромолекул с третичной структурой в сложный комплекс. Например, гемоглобин крови человека представляет комплекс из четырех макромолекул белка.
Такая сложность структуры белковых молекул связана с разнообразием функций, свойственных этим биополимерам.
Нарушение природной структуры белка называют денатурацией
. Она может происходить под воздействием температуры, химических веществ, лучистой энергии и других факторов. При слабом воздействии распадается только четвертичная структура, при более сильном - третичная, а затем - вторичная, и белок остается в виде полипептидной цепи.
Этот процесс частично обратим: если не нарушена первичная структура, то денатурированный белок способен восстанавливать свою структуру. Отсюда следует, что все особенность строение макромолекулы белка определяются его первичной структурой.
Кроме простых белков , состоящих только из аминокислот, есть еще и сложные белки
СТАТИЧЕСКАЯ БИОХИМИЯ
Глава IV .2.
Белки
Белки – неразветвляющиеся полимеры, минимальная структурная единица которых – аминокислота (АК). Аминокислоты соединены между собой пептидной связью. В природе встречается гораздо больше АК, чем входит в состав животных и растительный белков. Так, множество «небелковых» АК содержится в пептидных антибиотиках или являются промежуточными продуктами обмена белков. В состав белков входит 20 АК в альфа-форме, расположенных в различной, но строго определенной для каждого белка последовательности.
Классификация АК
По химическому строению
1) Алифатические – глицин (Гли), аланин (Ала), валин (Вал), лейцин (Лей), изолейцин (Илей);
2) Оксикислоты – серин (Сер), треанин (Тре);
3) Дикарбоновые – аспарагин (Асп), глутамин (Глу), аспарагиновая кислота (Аск), глутаминовая кислота (Глк);
4) Двуосновные – лизин (Лиз), гистидин (Гис), аргинин (Арг);
5) Ароматические – фениналанин (Фен), тирозин (Тир), триптофан (Три);
6) Серосодержащие – цистеин (Цис), метионин (Мет).
По биохимической роли:
1) глюкогенные – через ряд химических превращений поступают на путь гликолиза (окисления глюкозы) – Гли, Ала, Тре, Вал, Аск, Глк, Арг, Гис, Мет.
2) кетогенные – участвуют в образовании кетоновых тел - Лей, Илей, Тир, Фен.
По заменимости:
1) Незаменимые – не синтезируются в организме – Гис, Иле, Лей, Лиз, Мет, Фен, Тре, Три, Вал, а у молодняка Арг, Гис.
2) Заменимые – остальные.
За счет наличияв молекуле АК одновременно аминной и карбоксильной групп этим соединениям присущи кислотно-основные свойства. В нейтральной среде АК существуют в виде биполярных ионов- цвиттер-ионов т.е.
не NH 2 – R – COOH , аNH 3 + – R - COO –
Образование пептидной связи . Если карбоксильная группа одной АК ацилирует аминогруппу другой АК, от образуется амидная связь, которую называют пептидной. Т. о. пептиды – это соединения, образованные из остатков альфа-АК, соединенных между собой пептидной связью .
Данная связь достаточно стабильна и разрыв ее происходит лишь при участии катализаторов – специфических ферментов. Посредством такой связи АК объединяются в достаточно длинные цепочки, которые носят название полипептидных. Каждая такая цепь содержит на одном конце АК со свободной аминогруппой – это N -концевой остаток, и на другом с карбоксильной группой – С-концевой остаток.
Полипептиды, способные самопроизвольно формировать и удерживать определенную пространственную структуру, которая называется конформацией, относят к белкам. Стабилизация такой структуры возможна лишь при достижении полипептидами определенной длины, поэтому белками обычно считают полипептиды молекулярной массой более 5 000 Да. (1Да равен 1/12 изотопа углерода). Только имея определенное пространственное строение, белок может функционировать.
Функции белков
1) Структурная (пластическая) – белками образованы многие клеточные компоненты, а в комплексе с липидами они входят в состав клеточных мембран.
2) Каталитическая – все биологические катализаторы – ферменты по своей химической природе являются белками.
3) Транспортная – белок гемоглобин транспортирует кислород, ряд других белков образуя комплекс с липидами транспортируют их по крови и лимфе (пример: миоглобин, сывороточный альбумин).
4) Механохимическая – мышечная работа и иные формы движения в организме осуществляются при непосредственном участии сократительных белков с использованием энергии макроэргических связей (пример: актин, миозин).
5) Регуляторная – ряд гормонов и других биологически активных веществ имеют белковую природу (пр.: инсулин, АКТГ).
6) Защитная – антитела (иммуноглобулины) являются белками, кроме тогооснову кожи составляет белок коллаген, а волос – креатин. Кожа и волосы защищают внутреннюю среду организма от внешних воздействий. В состав слизи и синовиальной жидкости входят мукопротеиды.
7) Опорная – сухожилия, поверхности суставов соединения костей образованы в значительной степени белковыми веществами (пр.: коллаген, эластин).
8) Энергетическая – аминокислоты белков могут поступать на путь гликолиза, который обеспечивает клетку энергией.
9) Рецепторная – многие белки участвуют в процессах избирательного узнавания (рецепторы).
Уровни организации белковой молекулы.
В современной литературе принято рассматривать4 уровня организации структуры молекулы белка.
Последовательность аминокислотных остатков, соединенных между собой пептидной связью называют первичным уровнем организации белковой молекулы. Она кодируется структурным геном каждого белка. Связи: пептидная и дисульфидные мостики между относительно близко расположенными остатками цистеинов. Это ковалентные взаимодействия, которые разрушаются только под действием протеолитических ферментов (пепсин, трипсин и т.д.).
Вторичной структурой называют пространственное расположение атомов главной цепи молекулы белка . Существует три типа вторичной структуры: альфа-спираль, бета-складчатость и бета-изгиб. Образуется и удерживается в пространстве за счет образования водородных связей между боковыми группировками АК основной цепи. Водородные связи образуются между электроотрицательными атомами кислорода карбонильных групп и атомами водорода двух аминокислот.
Альфа-спираль – это пептидная цепь штопорообразно закрученная вокруг воображаемого цилиндра. Диаметр такой спирали 0,5 А. В природных белках обнаружена только правая спираль. Некоторые белки (инсулин) имеют две параллельные спирали. Бета-складчатость – полипептидная цепь собрана в равнозначные складки. Бета-изгиб – образуется между тремя аминокислотами за счет водородной связи. Он необходим для изменения пространственного расположения полипептидной цепи при образовании третичной структуры белка.
Третичная структура – это свойственный данному белку способ укладки полипептидой цепи в пространстве . Это основа функциональности белка. Она обеспечивает стабильность обширных участков белка, состоящих из множества аминокислотных остатков и боковых групп. Такие упорядоченные в пространстве участки белка формируют активные центры ферментов или зоны связывания и повреждение третичной структуры приводит к утрате функциональной активности белка.
Стабильность третичной структуры зависит в основном от нековалентных взаимодействий внутри белковой глобулы – преимущественно водородных связей и ван-дер-ваальсовых сил. Но некоторые белки дополнительно стабилизируются за счет таких ковалентных взаимодействий как дисульфидные мостики межу остатками цистеина.
Большинство белковых молекул имеют участки как альфа-спирали так и бета-складчатости. Но чаще по форме третичной структуры разделяют глобулярные белки – построенные преимуществено из альфа-спиралей и имеющеие форму шара или элипса (большинство ферментов). И фибрилярные – состоящие пеимущественно из бета-складчатости и имеющие сплющенную или нитевидную формы (пепсин, белки соединительной такни и хряща).
Размещение в пространстве взаимодействующих между собой субъединиц, образованных отдельными полипептидными цепями, называется четвертичной структурой . Т.е. в формировании четвертичной структуры участвуют не пептидные цепи сами по себе, а глобулы, образованные каждой из этих цепей в отдельности. Четвертичная структура – это высший уровень организации белковой молекулы и он присущ далеко не всем белкам. Связи, формирующие эту структуру нековалентные: водородные, электростатического взаимодействия.
Фундаментальный принцип молекулярной биологии: последовательность аминокислотных остатков полипептидной цепи белка несет в себе всю информацию, которая необходима для формирования определенной пространственной структуры. Т.е. имеющаяся в данном белке аминокислотная последовательность предопределяет образование альфа- или бета-конформации вторичной структуры за счет образования между этими АК водородных или дисульфидных связей и в дальнейшем формирование глобулярной или фибрилярной структуры также за счет нековалентных взаиомдействий между боковыми учатками определенных аминокислот.
Физико-химические свойства
Растворы белка относятся к растворам ВМС и обладают рядом свойств гидрофильных коллоидов: медленной диффузией, высокой вязкостью, опаслеценцией, дают конус Тиндаля.
1) Амфотерность связана с наличием в молекуле белка катионообразующих групп – аминогрупп и анионообразующих – карбоксильных группу. Знак заряда молекулы зависит от количества свободных групп. Если преоблазают карбоксильные группы то заряд молекулы отрицательный (проявляются свойства слабой кислоты), если аминогруппы – то положительный (основные свойства).
Заряд белка также зависит от рН среды. В кислой среде молекула приобретаетположительный заряд, в щелочной – отрицательный.
[ NH 3 + - R – COO - ] 0
pH > 7 [ OH - ]7 >pH [ H + ]
[ NH 2 - R – COO - ] - [ NH 3 + - R – COOH] +
Значение рН при котором число разноименных зарядов в белковой молекуле одинаково, т. е. суммарный заряд равен нулю называется изоэлектрической точкой данного белка. Устойчивость белковой молекулы к воздействию физических и химических факторов в изоэлектрической точке наименьшая.
Большинство природных белков содержат значительное количество дикарбоновых аминокислот и поэтому относятся к кислым белкам. Их изоэлектрическая точка лежит в слабокислой среде.
2) Растворы белков обладают буферными свойствами за счет их амфотерности.
3) Растворимость . Поскольку молекула белка содержит полярные амино – и карбоксильные группы, то в растворе поверхностные остатки АК гидратируются – происходит образование коацервата .
4) Коацервация - слияние водных оболочек нескольких частиц, без объединения самих частиц.
5) Коагуляция – склеивание белковых частиц и выпадение их в осадок. Это происходит при удаленииих гидратной оболочки. Для этого достаточно изменить структуручастицы белка, так, чтобы ее гидрофильные группы, которые связывают воду растворителя, оказались внутри частицы. Реакции осаждения балка в растворе делятся на две группы: обратимые (высаливание) и необратимые (денатурация).
6) Денатурацией называется существенное изменение вторичной и третичной структуры белка, т. е. Нарушение системы нековалентных взаимодействий, не затрагивающее его ковалентной (первичной) структуры. Денатурированный белок лишен всякой биологической активности в клетке и в основном используется как источник аминокислот. Денатурирующими агентами могут быть химические факторы: кислоты, щелочи, легко гидратирующие соли, органические растворители, различные окислители. К физическим факторам могут быть отнесены: действие высокого давления, многократное замораживание и оттаивание, ультразвуковые волны, УФ-лучи, ионизирующая радиация. Но наиболее распространенным физическим фактором денатурации белка является повышение температуры.
В ряде случаев денатурированный белок в клетке может быть подвергнут ренатурации, т. е. свернут обратно в первоначальную пространственную структуру. Этот процесс происходит при участии специфических белков, так называемых белков теплового шока (heat shock proteins или hsp ) молекулярной массой 70 кДа. Данные белки синтезируются в клетках в большом количествепри воздействии на нее (или весь организм) неблагоприятных факторов, в частности повышенной температуры. Присоединяясь к развернутой полипептидной цепи hsp 70 быстро сворачивают ее в правильную первоначальную структуру.
Классификация белков
По растворимости: водорастворимые, солерстворимые, спирторастворимые, нерастворимые и пр.
По конформационной структуре : фибриллярные, глобулярные.
По химическому строению: протеины – состоят только из аминокислот, протеиды – помимо АК имеют в составе небелковую часть (углеводы, липиды, металлы, нуклеиновые кислоты)
Протеины :
1) Альбумины – растворимы в воде, не растворимы в конц. растворах солей. р I = 4.6-4.7. Существуют альбумины молока, яиц, сыворотки крови.
2) Глобулины – не растворимы в воде, растворимы в солевых растворах. Имунноглобулины .
3) Гистоны – растворимы в воде, в слабоконцентрированных кислотах. Обладают выраженными основными свойствами. Это ядерные белки, они связаны с ДНК и РНК.
4) Склеропротеины – белки опорных тканей (хрящей, костей), шерсти, волос. Не растворимы в воде, слабых кислотах и щелочах.
а) коллагены – фибрилярные белки соединительной ткани. При длительном кипячении они растворяются в воде и при застудневании образуется желатин.
б) эластины– белки связок и сухожилий. По свойствам похожи на коллагены, но подвергаются гидролизу под действием ферментов пищеварительного сока;
в) кератин – входит в состав волос, перьев, копыт;
г) фиброин – белок шелка, в совем составе содержит много серина;
д) проламины и глютенины – белки растительного происхождения.
Протеиды
Помимо АК содержат простетическую группу и в зависимости от ее химической природы они классифицируются на:
1) Нуклеопротеиды – простетическая група – нуклеиновые кислоты. Среди многочисленных классов нуклеопротеидов наиболее изученными являются рибосомы, состоящие из нескольких молекул РНК и рибосомных белков, и хроматин – основной нуклеопротеид эукариотических клеток, состоящий из ДНК и структурообразующих белков – гистонов (содержатся в клеточном ядре и митохондриях) (подробнее см. главы "Нуклеиновые кислоты" и "Матричный биосинтез").
2) Гемопротеиды - небелковый компонент этих протеидов – гем, построен из четырех пиррольных колец, с ними связан ион двухвалентного железа (через атомы азота). К таким белка относятся: гемоглобин, миоглобин, цитохромы. Этот класс белков еще называют хромопротеиды, поскольку гем является окрашенным соединением. Гемоглобин – транспорт кислорода. Миоглобин – запасание кислорода в мышцах. Цитохромы (ферменты) – катализ окислительно-восстановаительных реакций и электронный транспорт в дыхательной цепи.
(Подробнее см. приложение 1).
3) Металлопротеиды – в состав простетической группы входят металлы. Хлорофилл – содержит гем, но вместо железа – магний. Цитохром а – содержит медь, сукцинатдегидрогеназа и др. ферменты содержат негеминовое железо (ферродоксин ).
4) Липопротеиды – содержат липиды, входят в состав клеточных мембран
5) Фосфопротеиды – содержат остаток фосфорной кислоты
6) Глюкопротеиды – содержат сахара
ЛИТЕРАТУРА К ГЛАВЕ IV .2.
1. Балезин С. А. Практикум по физической и коллоидной химии // М:. Просвещение, 1972, 278 с.;
2. Бышевский А. Ш., Терсенов О. А. Биохимия для врача // Екатеринбург: Уральский рабочий, 1994, 384 с.;
3. Кнорре Д. Г., Мызина С. Д. Биологическая химия. – М.: Высш. шк. 1998, 479 с.;
4. Молекулярная биология. Структура и функции белков /Под ред. А. С. Спирина // М.: Высш. шк., 1996, 335 с.;
6. Равич – Щербо М. И., Новиков В. В. Физическая и коллоидная химия // М:. Высш. шк., 1975,255 с.;
7. Филиппович Ю. Б., Егорова Т. А., Севастьянова Г. А. Практикум по общей биохимии // М.: Просвящение, 1982, 311с.;














 Всеволод большое гнездо как правитель
Всеволод большое гнездо как правитель Как заполняются электронные уровни, подуровни и орбитали по мере усложнения атома
Как заполняются электронные уровни, подуровни и орбитали по мере усложнения атома Самые первые спички в мире
Самые первые спички в мире