В электрохимических методах измерения концентрации используют электрохимическую ячейку. Простейшая ячейка состоит из пары электродов, погруженных в раствор электролита. Раствор электролита помещен в один сосуд или в два, соединенных между собой мостиком с электролитом (ячейка с переносом). Электроды могут быть соединены непосредственно между собой проводником (внутренний электролиз) или проводниками через источник питания (внешний электролиз).
Механизм переноса электричества в разных участках электрической цепи различен. По проводникам электрический заряд переносится электронами, в растворе – ионами. На границе раздела фаз происходит изменение механизма проводимости в результате протекания гетерогенной окислительно-восстановительной реакции. Её называют электрохимической или электродной реакцией, то есть реакцией, связанной с обменом зарядами между химическими соединениями, находящимися в разных фазах – твердой (поверхность электрода) и жидкой (раствор электролита).
Есть химические соединения в растворе, которые легко отдают электроны электроду, изготовленному из определенного материала, например платины или графита, то есть окисляются на нём. Такой электрод называют анодом. На поверхности анода образуется окислитель, который может на нём остаться (адсорбироваться), раствориться в материале анода (ртутном аноде) или диффундировать в раствор электролита под действием сил диффузии (градиента концентрации).
Например, в растворе CuCl 2
2Cl - - 2e = Cl 2
(Red 1 - ne = Ox 1)
Раствор Pt-электрод
Cl - → ←Cl 2
Образующийся на поверхности платинового электрода газообразный Cl 2 будет диффундировать в раствор электролита.
Есть также в растворе химические соединения, которые легко принимают электроны от электрода, т.е. восстанавливаются на нем. Такой электрод называют катодом. На поверхности катода образуется восстановитель, который может на нём остаться (адсорбироваться), раствориться в материале анода (ртутном катоде) или диффундировать в раствор электролита под действием сил диффузии.
Например, в растворе CuCl 2
Cu 2+- + 2e = Cu 0
(Ox 2 + ne = Red 2)
раствор Hg-электрод
Cu 2+ →Cu 0 → Cu 0 (Hg)
Образующиеся на поверхности ртутного электрода атомы меди будут диффундировать в глубь ртути, растворяясь в ней с образованием амальгамы.
И на аноде и на катоде образуются новые химические соединения, которых раньше в растворе не было. Если происходит перенос заряда из одной фазы в другую, то на межфазной границе устанавливается электрический потенциал (энергия).
Если электроды соединить проводником, то при достаточной разности потенциалов между электродами сопротивление раствора движению зарядов будет преодолено и через раствор потечет электрический ток (движение зарядов). Этот ток может быть измерен.
Электрохимические методы химического анализа основаны на использовании явлений и процессов, протекающих на поверхности электрода, в приэлектродном слое или в растворе электролита, связанных с химической природой и содержанием компонентов в растворе.
Измеряют электрические свойства системы электрод – электролит (потенциал электрода, силу электрического тока, количество электричества, электрическую проводимость и др.), Все рассмотренные электрические величины зависят от концентрации каких-либо компонентов раствора электролита. Следовательно, любая из них – электрическая проводимость электролита, потенциал электрода, сила электрического тока, ёмкость двойного электрического слоя и другие, может служить аналитическим сигналом, если она функционально связана с концентрацией определяемого компонента в анализируемом растворе и поддается измерению. Измеренные значения электрических свойствиспользуют для количественного и иногда для качественного химического анализа состава вещества.
Существуют различные классификации электрохимических методов определения концентрации компонента. Например, методы могут быть классифицированы следующим образом.
1. Методы, основанные на протекании электродной реакции.
1.1. Методы, основанные на прохождении электрического тока через электрохимическую ячейку:
-- вольтамперометрия – метод, основанный на измерении силы диффузионного тока электроокисления или электровосстановления определяемого компонента при определённом значении потенциала индикаторного электрода;
-- кулонометрия – метод, основанный на измерении количества электричества (закон Фарадея), затраченного на электрохимическую реакцию определяемого компонента;
-- электрогравиметрия – метод, основанный на измерении массы определяемого компонента, выделенного на электроде при прохождении электрического тока через раствор электролита (закон Фарадея);
1.2.Методы, основанные на измерении разности потенциалов между парой электродов при протекании ничтожно малых токов в растворе:
-- потенциометрия – метод, основанный на измерении разности потенциалов индикаторного электрода и электрода сравнения;
2. Методы, не связанные с протеканием электродной реакции:
-- кондуктометрия – метод, основанный на измерении удельной электрической проводимости раствора, зависящей от природы и концентрации растворённых в нём компонентов.
Концентрацию определяемого компонента в пробе вещества объекта химического анализа находят, как и в любом другом физическом методе химического анализа, из градуировочного графика.
Внимание. Средства измерения электрических свойств веществ используют также в химических методах количественного химического анализа, таких как титриметрия, с целью фиксирования при проведении химической реакции эквивалентного объёма титранта. Это так называемый инструментальный (безиндикаторный) способ фиксирования точки эквивалентности. С помощью средства измерения электрических свойств веществ измеряют соответствующее электрическое свойство определяемого компонента, меняющееся при добавлении каждой порции титранта. В точке эквивалентности интенсивность измеряемого свойства резко изменяется и этот момент можно зафиксировать путем построения и графической обработки кривой титрования, построенной в координатах “измеренное значение электрического свойства – добавленный объём титранта” . Концентрацию определяемого компонента находят из закона эквивалентов. Это расширяет возможности титриметрических методов в анализе окрашенных, мyтных растворов, агрессивных сред и т.д., где применение цветных индикаторов для фиксирования точки эквивалентности невозможно. Методы титрования в этом случае называются так: метод потенциометрического титрования, метод кондуктометрического титрования, метод амперометрического титрования и т.д. По способу сравнения с эталоном эти методы относятся к химическим методам количественного химического анализа.
Характерными достоинствами электрохимических методов химического анализа являются низкий предел определения, экспрессность анализа, легкость проведения измерений средствами измерения, возможность автоматизации и непрерывности химического анализа. Однако процессы, происходящие в электрохимических ячейках, достаточно сложны для понимания и интерпретации полученных результатов из-за их неоднозначности, поэтому этими методами практически невозможно провести качественный анализ пробы вещества, что ограничивает возможности электрохимических методов химического анализа веществ.
Недостатком электрохимических методов анализа по сравнению с химическими методами количественного анализа является их сравнительно невысокая точность (погрешность анализа ~ 10 %), однако, некоторые методы (кулонометрия, электрогравиметрия) относятся к высокоточным (погрешность анализа ~ 0,01 %).
Электрохимические методы анализа - это совокупность методов качественного и количественного анализа, основанных на электрохимических явлениях, происходящих в исследуемой среде или на границе раздела фаз и связанных с изменением структуры, химического состава или концентрации анализируемого вещества.
Разновидностями метода являются электрогравиметрический анализ (электроанализ), внутренний электролиз, контактный обмен металлов (цементация), полярографический анализ, кулонометрия и др. В частности, электрогравиметрический анализ основан на взвешивании вещества, выделяющемся на одном из электродов. Метод позволяет не только проводить количественные определения меди, никеля, свинца и др., но и разделять смеси веществ.
Кроме того, к электрохимическим методам анализа относят методы, основанные на измерении электропроводности (кондуктометрия) или потенциала электрода (потенциометрия). Некоторые электрохимические методы применяются для нахождения конечной точки титрования (амперометрическое титрование, кондуктометрическое титрование, потенциометрическое титрование, кулонометрическое титрование).
Различают прямые и косвенные электрохимические методы. В прямых методах используют зависимость силы тока (потенциала и т.д.) от концентрации определяемого компонента. В косвенных методах силу тока (потенциал и т. д.) измеряют с целью нахождения конечной точки титрования определяемого компонента подходящим титрантом, т.е. используют зависимость измеряемого параметра от объема титранта.
Для любого рода электрохимических измерений необходима электрохимическая цепь или электрохимическая ячейка, составной частью которой является анализируемый раствор.
Электрохимические методы классифицируют в зависимости от типа явлений, замеряемых в процессе анализа. Различают две группы электрохимических методов:
1. Методы без наложения постороннего потенциала, основанные на измерении разности потенциалов, который возникает в электрохимической ячейке, состоящей из электрода и сосуда с исследуемым раствором. Эту группу методов называют потенциометрическими. В потенциометрических методах используют зависимость равновесного потенциала электродов от концентрации ионов, участвующих в электрохимической реакции на электродах.
2. Методы с наложением постороннего потенциала, основанные на измерении: а) электрической проводимости растворов - кондуктометрия ; б) количества электричества, прошедшего через раствор - кулонометрия ; в) зависимости величины тока от приложенного потенциала - вольт-амперометрия ; г) времени, необходимого для прохождения электрохимической реакции - хроноэлектрохимические методы (хроновольтамперометрия, хронокондуктометрия). В методах этой группы на электроды электрохимической ячейки налагают посторонний потенциал.
Основным элементом приборов для электрохимического анализа является электрохимическая ячейка. В методах без наложения постороннего потенциала она представляет собой гальванический элемент , в котором вследствие протекания химических окислительно-восстановительных реакций возникает электрический ток. В ячейке типа гальванического элемента в контакте с анализируемым раствором находятся два электрода - индикаторный электрод, потенциал которого зависит от концентрации вещества, и электрод с постоянным потенциалом - электрод сравнения, относительно которого измеряют потенциал индикаторного электрода. Измерение разности потенциалов производят специальными приборами - потенциометрами.
В методах с наложением постороннего потенциала применяют электрохимическую ячейку , названную так потому, что на электродах ячейки под действием наложенного потенциала происходит электролиз - окисление или восстановление вещества. В кондуктометрическом анализе используют кондуктометрическую ячейку, в которой замеряют электрическую проводимость раствора. По способу применения электрохимические методы можно классифицировать на прямые, в которых концентрацию веществ измеряют по показанию прибора, и электрохимическое титрование, где индикацию точки эквивалентности фиксируют с помощью электрохимических измерений. В соответствии с этой классификацией различают потенциометрию и потенциометрическое титрование, кондуктометрию и кондуктометрическое титрование и т.д.
Приборы для электрохимических определений кроме электрохимической ячейки, мешалки, нагрузочного сопротивления включают устройства для измерения разности потенциалов, тока, сопротивление раствора, количества электричества. Эти измерения могут осуществляться стрелочными приборами (вольтметр или микроамперметр), осциллографами, автоматическими самопишущими потенциометрами. Если электрический сигнал от ячейки очень слабый, то его усиливают с помощью радиотехнических усилителей. В приборах методов с наложением постороннего потенциала важной частью являются устройства для подачи на ячейку соответствующего потенциала стабилизированного постоянного или переменного тока (зависит от типа метода). Блок электропитания приборов электрохимического анализа включает обычно выпрямитель и стабилизатор напряжения, который обеспечивает постоянство работы прибора.
Потенциометрия объединяет методы, основанные на измерении эдс обратимых электрохимических цепей, когда потенциал рабочего электрода близок к равновесному значению.
Вольтамперометрия основана на исследовании зависимости тока поляризации от напряжения, прикладываемого к электрохимической ячейке, когда потенциал рабочего электрода значительно отличается от равновесного значения. Широко используется для определения веществ в растворах и расплавах (например, полярография, амперометрия).
Кулонометрия объединяет методы анализа, основанные на измерении количества вещества, выделяющегося на электроде в процессе электрохимической реакции в соответствии с законами Фарадея . При кулонометрии потенциал рабочего электрода отличается от равновесного значения.
Кондуктометрический анализ основан на изменении концентрации вещества или химического состава среды в межэлектродном пространстве; он не связан с потенциалом электрода, который обычно близок к равновесному значению.
Диэлектрометрия объединяет методы анализа, основанные на измерении диэлектрической проницаемости вещества, обусловленной ориентацией в электрическом поле частиц (молекул, ионов), обладающих дипольным моментом. Диэлектрометрическое титрование используют для анализа растворов.
Описание работы
Современные отрасли производства и социальной жизни людей ставят свои специфические задачи перед физико-химическими методами анализа по контролю качества продукции. Одними из основных физико-химических методов анализа являются электрохимические методы анализа.
Этими методами можно быстро и достаточно точно определить многие показатели качества продукции.
Электрохимические методы анализа состава вещества широко используются в различных отраслях промышленности. Они позволяют автоматизировать получение результатов о качестве продукции и исправлять нарушения, не останавливая производство. В пищевой промышленности этими методами определяют кислотно-щелочной баланс продукта, наличие вредных и токсичных веществ и другие показатели, влияющие не только на качество, но и на безопасность пищи.
Оборудование, предназначенное для проведения электрохимических анализов, отличается относительной дешевизной, доступностью и простотой в использовании. Поэтому эти методы имеют широкое применение не только в специализированных лабораториях, но и на многих производствах.
В связи с этим целью данной ку
ВВЕДЕНИЕ 2
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ 3
1.1 Общая характеристика физико-химических методов анализа 3
1.2 Характеристика электрохимических методов 4
1.3 Классификация электрохимических методов анализа 5
2 ЭКСПЕРЕМЕНТАЛЬНО-ПРАКТИЧЕСКАЯ ЧАСТЬ 15
ЗАКЛЮЧЕНИЕ 21
СПИСОК ЛИТЕРАТУРЫ 22
Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru
Министерство образования и науки РФ
Федеральное государственное бюджетное образовательное учреждение
высшего образования
«Иркутский национальный исследовательский технический университет»
Кафедра металлургии цветных металлов
(наименование кафедры)
«Электрохимические методы исследования»
Реферат по дисциплине
«Физико-химические методы исследования металлургических процессов»
Выполнил студент группы МЦМ-16-1
Захаренков Р. И.
Проверил преподаватель кафедры МЦМ
Кузьмина М.Ю.
Иркутск 2017 г.
ВВЕДЕНИЕ
Электрохимия - раздел физической химии, который рассматривает системы, содержащие ионы (растворы или расплавы электролитов) и процессы, протекающие на границе двух фаз с участием заряженных частиц.
Первые представления о взаимосвязи химических и электрических явлений были известны в XVIII веке, так как было выполнено огромное количество физико-химических экспериментов с электрическим и грозовыми разрядами, с зарядами, находящимися в лейденских банках, но все они имели случайный характер из-за отсутствия постоянного мощного источника электрической энергии. Зарождение электрохимии связано с именами Л. Гальвани и А. Вольта. Занимаясь исследованием физиологических функций лягушки, Гальвани случайно создал электрохимическую цепь. Она состояла из двух различных металлов и препарированной лапки лягушки. Лапка одновременно являлась электролитом и индикатором электрического тока, но вывод был дан неправильный, т. е., согласно Гальвани, этот электрический ток, который возникал в цепи, имел животное происхождение, т. е. был связан с функциональными особенностями организма лягушки (теория «животного электричества»).
Правильное толкование опытам Гальвани дал А. Вольта. Он создал первую батарею гальванических элементов - вольтов столб. Элементы батареи состояли из медных и цинковых дисков, а электролитом служил пропитанный соленой водой или кислотой губчатый материал. Именно такое соединение позволило получить электрический ток. Вскоре трудами великих ученых А. Вольта, Дж. Даниэля, Б. С. Якоби, П. Р. Багратиона, Г. Плантэ и др. появились удобные в работе мощные гальванические элементы и аккумуляторы. Затем А. Вольта разработал ряд напряжений металлов. Если два различных металла привести в соприкосновение, а затем разъединить, то при помощи физических средств, например, электроскопа, можно увидеть, что один металл приобрел положительный заряд, а другой - отрицательный. Этот ряд металлов, в котором каждый предшествующий металл заряжается положительно, но после контакта с любым последующим, т. е. ряд Вольта, оказался аналогичным ряду напряжений.
Далее, в начале XIX века, был разработан электролиз, а М. Фарадей установил количественные законы электролиза. Большой вклад в развитие электрохимии внесли ученые: С. А. Аррениус, В. Ф. Оствальд, Р. А. Колли, П. Дебай, В. Нернст, Г. Гельмгольц и др. Сейчас электрохимия делится на теоретическую и прикладную. Благодаря использованию электрохимических методов, она связана с другими разделами физической химии, а также с аналитической химией и другими науками.
электрохимический потенциометрия кондуктометрия кулонометрия
1 . ЭЛЕТРОХИМИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ
Необходимость в использовании разнообразных методов для исследования электрохимических процессов обусловлена широкой областью изменения скорости переноса электрона в электродных реакциях. Каждый из методов имеет некоторый предел по определяемому значению плотности тока обмена, выше которого электрохимические параметры электродной реакции определить нельзя. Применительно к каждому конкретному объекту необходимо выбрать тот метод, который дает максимальный объем надежной информации. При проведении электрохимических исследований необходимо знать химический состав исходных веществ и продуктов реакции. Для определения состава электролита используют различные физико-химические методы: спектрофотометрический, потенциометрический, аналитический и другие. При проведении электрохимических исследований необходимо соблюдать следующие условия.
1. Максимальная чистота используемых реактивов; состав электродов должен быть строго известен, как известно и состояние их поверхностей. Следует следить за тем, чтобы в процессе измерений поверхность электродов не претерпевала изменений.
2. Конструкция электрохимической ячейки и расположенный в ней электродов должны обеспечивать равномерное распределение тока по всей поверхности рабочего электрода.
3. Измерение проводить при строго контролируемой температуре.
4. Поддерживать постоянные давления и состав газовой фазы над электролитом. Как правило, исследования проводят в среде инертного газа (N 2 , Ar, Ne, He H 2), поскольку кислород газовой фазы может оказывать существенное влияние на механизм процесса.
5. Необходимо обеспечить такие условия эксперимента, при которых падение потенциала в диффузной части двойного электрического слоя было бы минимальным или точно известным. Для снижения этого потенциала используют, как правило, фоновый электролит, концентрация которого должна быть не менее, чем в 20 раз выше, чем у основного вещества. Однако предварительно следует убедиться, что фоновый электролит не искажает поляризационной кривой изучаемой реакции.
6. Точное измерение потенциала рабочего электрода. Для этого необходимо устранить диффузионный потенциал между исследуемым электролитом и электролитом электрода сравнения. Этот потенциал принимает максимальное значение при приближении к предельному току и может, существенно исказить результаты измерений. Для устранения диффузионного потенциала между исследуемым электролитом и электролитом электрода сравнения желательно: а) выбрать электрод сравнения, который имеет тот же электролит по составу, что и исследуемый. Например, при исследованиях в хлоридных растворах удобно применять хлор-серебрянный, каломельный, хлорный электроды; в кислых сульфатных растворах - ртутно-сульфатные электроды и т.п.; б) использовать электрод сравнения с таким электролитом, на границе которого с исследуемым электролитом диффузионный потенциал может быть рассчитан по известным формулам.
При измерении в растворах с постоянной ионной силой, а при больших концентрациях фона - с постоянной ионной концентрацией можно, в принципе, использовать любой электрод сравнения. Диффузионный потенциал в этом случае может быть и весьма велик, но и постоянен - его можно рассчитать или определить экспериментально.
Во всех случаях изучения кинетики электрохимических процессов необходимо измерение плотности тока. Обычно начинают с того, что выясняют методами аналитической химии, кулонометрии, протекает ли на электроде только одна изучаемая реакция или она осложнена побочными. В случае протекания побочных реакций, надо выяснить, какая доля тока приходится только на осуществление изучаемой реакции (построить так называемую парциальную поляризационную характеристику для изучаемой реакции).
Наиболее просто механизм электродной реакции можно интерпретировать лишь в случае, когда исходное вещество превращается в один продукт со 100%-ным выходом по току. Проверка реакции на соответствие закону Фарадея или проведение кулонометрических измерений позволяет одновременно определить число электронов, участвующих в суммарной электродной реакции. Знание состава исходного вещества и продукта реакции, а также общего числа переносимых электронов, дает возможность записать уравнение суммарной электродной реакции.
Следующим шагом в изучении механизма электродной реакции является выяснение того, какая стадия является лимитирующей.
Если лимитирующей стадией является стадия разряда -ионизации, а все другие протекают обратимо, то основные кинетические параметры процесса можно определить графически или аналитически, применяя к поляризационным характеристикам уравнения теории замедленного разряда .
1.1 Электрохимические методы анализа
Электрохимические методы анализа - это совокупность методов качественного и количественного анализа, основанных на электрохимических явлениях, происходящих в исследуемой среде или на границе раздела фаз и связанных с изменением структуры, химического состава или концентрации анализируемого вещества.
Различают прямые и косвенные электрохимические методы. В прямых методах используют зависимость силы тока (потенциала и т.д.) от концентрации определяемого компонента. В косвенных методах силу тока (потенциал и т. д.) измеряют с целью нахождения конечной точки титрования определяемого компонента подходящим титрантом, т.е. используют зависимость измеряемого параметра от объема титранта.
Для любого рода электрохимических измерений необходима электрохимическая цепь или электрохимическая ячейка, составной частью которой является анализируемый раствор.
Электрохимические методы классифицируют в зависимости от типа явлений, замеряемых в процессе анализа. Различают две группы электрохимических методов:
1. Методы без наложения постороннего потенциала, основанные на измерении разности потенциалов, который возникает в электрохимической ячейке, состоящей из электрода и сосуда с исследуемым раствором. Эту группу методов называют потенциометрическими. В потенциометрических методах используют зависимость равновесного потенциала электродов от концентрации ионов, участвующих в электрохимической реакции на электродах.
2. Методы с наложением постороннего потенциала, основанные на измерении:
а) Электрической проводимости растворов? кондуктометрия ;
б) Количества электричества, прошедшего через раствор? кулонометрия ;
в) Зависимости величины тока от приложенного потенциала? вольт-амперометрия ;
г) Времени, необходимого для прохождения электрохимической реакции - хроноэлектрохимические методы (хроновольтамперометрия, хронокондуктометрия).
В методах этой группы на электроды электрохимической ячейки налагают посторонний потенциал.
Основным элементом приборов для электрохимического анализа является электрохимическая ячейка. В методах без наложения постороннего потенциала она представляет собой гальванический элемент , в котором вследствие протекания химических окислительно-восстановительных реакций возникает электрический ток. В ячейке типа гальванического элемента в контакте с анализируемым раствором находятся два электрода - индикаторный электрод, потенциал которого зависит от концентрации вещества, и электрод с постоянным потенциалом - электрод сравнения, относительно которого измеряют потенциал индикаторного электрода. Измерение разности потенциалов производят специальными приборами - потенциометрами .
В методах с наложением постороннего потенциала применяют электрохимическую ячейку , названную так потому, что на электродах ячейки под действием наложенного потенциала происходит электролиз - окисление или восстановление вещества. В кондуктометрическом анализе используют кондуктометрическую ячейку, в которой замеряют электрическую проводимость раствора. По способу применения электрохимические методы можно классифицировать на прямые, в которых концентрацию веществ измеряют по показанию прибора, и электрохимическое титрование, где индикацию точки эквивалентности фиксируют с помощью электрохимических измерений. В соответствии с этой классификацией различают потенциометрию и потенциометрическое титрование, кондуктометрию и кондуктометрическое титрование и т.д.
Приборы для электрохимических определений кроме электрохимической ячейки, мешалки, нагрузочного сопротивления включают устройства для измерения разности потенциалов, тока, сопротивление раствора, количества электричества. Эти измерения могут осуществляться стрелочными приборами (вольтметр или микроамперметр), осциллографами, автоматическими самопишущими потенциометрами. Если электрический сигнал от ячейки очень слабый, то его усиливают с помощью радиотехнических усилителей. В приборах методов с наложением постороннего потенциала важной частью являются устройства для подачи на ячейку соответствующего потенциала стабилизированного постоянного или переменного тока (зависит от типа метода). Блок электропитания приборов электрохимического анализа включает обычно выпрямитель и стабилизатор напряжения, который обеспечивает постоянство работы прибора.
1.2 Потенциометрия
Потенциометрия основана на измерении разности электрических потенциалов, возникающих между разнородными электродами, опущенными в раствор с определяемым веществом. Электрический потенциал возникает на электродах при прохождении на них окислительно-восстановительной (электрохимической) реакции. Окислительно-восстановительные реакции протекают между окислителем и восстановителем с образованием окислительно-восстановительных пар, потенциал Е которых определяется по уравнению Нернста концентрациями компонентов пар [ок] и [вос]:
где Е° - стандартный электродный потенциал, В;
n - число электронов, участвующих в процессе.
Потенциометрические измерения проводят, опуская в раствор два электрода - индикаторный, реагирующий на концентрацию определяемых ионов, и стандартный электрод или электрод сравнения, относительно которого измеряется потенциал индикаторного. Применяют несколько видов индикаторных и стандартных электродов.
Электроды первого рода обратимы относительно ионов металла, из которого состоит электрод. При опускании такого электрода в раствор, содержащий катионы металла, образуется электродная пара: M n + /M .
Электроды второго рода чувствительны к анионам и представляют собой металл М, покрытый слоем нерастворимой его соли МА с анионом A -, к которому чувствителен электрод. При контакте такого электрода с раствором, содержащим указанный анион A -, возникает потенциал Е, величина которого зависит от произведения растворимости соли
ПР MA и концентрации аниона [A -] в растворе.
Электродами второго рода являются хлорсеребряный и каломельный. Насыщенные хлорсеребряный и каломельный электроды поддерживают постоянный потенциал и применяют в качестве электродов сравнения, по отношению к которым измеряется потенциал индикаторного электрода.
Инертные электроды - пластина или проволока, изготовленная из трудноокисляемых металлов - платины, золота, палладия. Применяются они для измерения Е в растворах, содержащих окислительно-восстановительную пару (например, Fe 3+ /Fe 2+).
Мембранные электроды различного типа имеют мембрану, на которой возникает мембранный потенциал Е. Величина Е зависит от разности концентраций одного и того же иона по разным сторонам мембраны. Простейшим и наиболее употребляемым мембранным электродом является стеклянный электрод.
Смешивание нерастворимых солей типа AgBr, AgCl, AgI и других с некоторыми пластмассами (каучуки, полиэтилен, полистирол) привело к созданию ион-селективных электродов на Br -, Cl -, I -, избирательно адсорбирующих из раствора указанные ионы вследствие правила Панета - Фаянса - Гана. Так как концентрация определяемых ионов вне электрода отличается от таковой внутри электрода, равновесия на поверхностях мембраны отличаются, что приводит к возникновению мембранного потенциала.
Для проведения потенциометрических определений собирают электрохимическую ячейку из индикаторного электрода сравнения, который опускают в анализируемый раствор и подсоединяют к потенциометру. Применяемые в потенциометрии электроды имеют большое внутреннее сопротивление (500-1000 МОм), поэтому существуют типы потенциометров представляют собой сложные электронные высокоомные вольтметры. Для измерения ЭДС электродной системы в потенциометрах применяют компенсационную схему, позволяющую уменьшить ток в цепи ячейки.
Наиболее часто потенциометры применяют для прямых измерений рН, показатели концентраций других ионов pNa, pK, pNH?, pCl и мВ. Измерения проводят, используя соответствующие ион-селективные электроды.
Для измерения рН применяют стеклянный электрод и электрод сравнения - хлорсеребряный. Перед проведением анализов необходимо проверить калибровку рН-метров по стандартным буферным растворам, фиксаналы которых прикладываются к прибору.
рН-метры помимо прямых определений рН, pNa, pK, pNH?, pCl и других позволяют проводить потенциометрическое титрование определяемого иона.
1.3 Потенциометрическое титрование
Потенциометрическое титрование проводят в тех случаях, когда химические индикаторы использовать нельзя или при отсутствии подходящего индикатора.
В потенциометрическом титровании в качестве индикаторов используют электроды потенциометра, опушенные в титруемый раствор. При этом применяют электроды, чувствительные к титруемым ионам. В процессе титрования изменяется концентрация ионов, что регистрируется на шкале измерительного пробора потенциометра. Записав показания потенциометра в единицах рН или мВ, строят график их зависимости от объема титранта (кривую титрования), определяют точку эквивалентности и объем титранта, израсходованный на титрование. По полученным данным строят кривую потенциометрического титрования.
Кривая потенциометрического титрования имеет вид, аналогичный кривой титрования в титриметрическом анализе. По кривой титрования определяют точку эквивалентности, которая находится в середине скачка титрования. Для этого проводят касательные к участкам кривой титрования и по середине касательной скачка титрования определяют точку эквивалентности. Наибольшее значение изменения ? рН/?V приобретает в точке эквивалентности.
Еще более точно точку эквивалентности можно определить методом Грана, по которому строят зависимость ? V/?Е от объема титранта. Методом Грана можно проводить потенциометрическое титрование, не доводя его до точки эквивалентности.
Потенциометрическое титрование применяют во всех случаях титриметрического анализа.
При кислотно-основном титровании используют стеклянный электрод и электрод сравнения. Поскольку стеклянный электрод чувствителен к изменениям рН среды, при их титровании на потенциометре регистрируются изменения рН среды. Кислотно-основное потенциометрическое титрование с успехом применяют при титровании слабых кислот и оснований (рК?8). При титровании смесей кислот необходимо, чтобы их рК отличались больше, чем на 4 единицы, в противном случае часть более слабой кислоты оттитровывается вместе с сильной, и скачок титрования выражен не четко.
Это позволяет использовать потенциометрию для построения экспериментальных кривых титрования, подбор индикаторов для титрования и определения констант кислотности и основности.
При осадительном потенциометрическом титровании применяют в качестве индикатора электрод из металла, составляющего с определяемыми ионами электродную пару.
При комплексометрическом титровании используют: а) металлический электрод, обратимый к иону определяемого металла; б) платиновый электрод при наличии в растворе окислительно-восстановительной пары. При связывании титрантом одного из компонентов редокс-пары меняется его концентрация, что вызывает изменения потенциала индикаторного платинового электрода. Применяются также обратное титрование избытка раствора ЭДТА, добавленного к соли металла, раствором соли железа (III).
При окислительно-восстановительном титровании применяют электрод сравнения и платиновый индикаторный электрод, чувствительный к окислительно-восстановительным парам.
Потенциометрическое титрование - один из наиболее употребляемых методов инструментального анализа вследствие простоты, доступности, селективности и широких возможностей.
1.4 Кондуктометрия. Кондуктометрическое титрование
Кондуктометрия основана на измерении электрической проводимости раствора. Если в раствор вещества поместить два электрода и подать на электроды разность потенциалов, то через раствор потечет электрический ток. Как и каждый проводник электричества, растворы характеризуются сопротивлением R и обратной ему величиной - электрической проводимостью L :
где R - сопротивление, Ом;
Удельное сопротивление, Ом. см;
S - площадь поверхности, см 2 .
где L - электрическая проводимость, Ом- 1 ;
R - сопротивление, Ом.
Кондуктометрический анализ проводят с помощью кондуктометров - приборов, измеряющих сопротивление растворов. По величине сопротивления R определяют обратную ему по величине электрическую проводимость растворов L .
Определение концентрации растворов осуществляют прямой кондуктометрией и кондуктометрическим титрованием. Прямая кондуктометрия используется для определения концентрации раствора по калибровочному графику. Для составления калибровочного графика замеряют электрическую проводимость серии растворов с известной концентрацией и строят калибровочный график зависимости электрической проводимости от концентрации. Затем измеряют электрическую проводимость анализируемого раствора и по графику определяют его концентрацию.
Чаще применяют кондуктометрическое титрование . При этом в ячейку с электродами помещают анализируемый раствор, ячейку помещают на магнитную мешалку и титруют соответствующим титрантом. Титрант добавляют равными порциями. После добавления каждой порции титранта замеряют электрическую проводимость раствора и строят график зависимости между электрической проводимостью и объемом титранта. При добавлении титранта происходит изменение электрической проводимости раствора в т.э. наступает перегиб кривой титрования.
От п одвижности ионов зависит электрическая проводимость раствора: чем выше подвижност ь ионов, тем больше электрическая проводимость раствора.
Кондуктометрическое титрование обладает рядом преимуществ. Его можно проводить в мутных и окрашенных средах, в отсутствии химических индикаторов. Метод обладает повышенной чувствительностью и позволяет анализировать разбавленные растворы веществ (до 10- 4 моль/дмі). Кондуктометрическим титрованием анализируют смеси веществ, т.к. различия в подвижности различных ионов существенны и их можно дифференцированно оттитровывать в присутствии друг друга.
Кондуктометрический анализ легко автоматизировать, если раствор титранта подавать из бюретки с постоянной скоростью, а изменение электрической проводимости раствора регистрировать на самописце.
Эта разновидность кондуктометрии получила название хроно - кондуктометрического анализа .
В кислотно-основном титровании кондуктометрическим путем можно определять сильные кислоты, слабые кислоты, соли слабых оснований и сильных кислот.
В осадительном кондуктометрическом титровании электрическая проводимость титруемых растворов сначала уменьшается или остается на некотором постоянном уровне вследствие связывания титруемого электролита в осадок, после т.э. при появлении избытка титранта - снова возрастает.
В комплексо метрическом кондуктометрическом титровании изменения электрической проводимости раствора наступают вследствие связывания катионов металла в комплекс с ЭДТА.
Окислительно-восстановительное кондуктометрическое титро - вание основано на изменении концентрации реагирующих ионов и появлении в растворе новых ионов, что изменяет электрическую проводимость раствора.
В последние годы получило развитие высокочастотная кондуктометрия , в которой электроды с раствором не контактируют, что важно при анализе агрессивных сред и растворов в закрытых сосудах.
Получила развитие два варианта - прямая высокочастотная кондуктометрия и высокочастотное титрование.
Прямая высокочастотная кондуктометрия применяется для определения влажности веществ, зерна, древесины, концентрации растворов в закрытых сосудах - ампулах, при анализе агрессивных жидкостей.
Высокочастотное титрование проводят на специальных титраторах - ТВ-6, ТВ-6Л.
Высокочастотное кондуктометрическое титрование проводят по типу кислотно-основного, окислительно-восстановительного или осадительного титрования в тех случаях, когда отсутствует подходящий индикатор или при анализе смесей веществ.
1.5 Кулонометрия. Кулонометрическое титрование
В кулонометрии вещества определяют измерением количества электричества, затраченное на их количественное электрохимическое превращение. Кулометрический анализ проводят в электролитической ячейке, в которую помещают раствор определяемого вещества. При подаче на электроды ячейки соответствующего потенциала происходит электрохимическое восстановление или окисление вещества. Согласно законам электролиза, открытым Фарадеем, количество вещества, прореагировавшего на электроде, пропорционально количеству электричества, прошедшего через раствор:
где g - масса, выделяющегося вещества, г;
n - количество электронов, переносимых в электродном процессе;
F - число Фарадея (F = 96485 Кл/моль);
I - сила тока, А;
t - время, с;
M - молярная масса выделяющегося вещества, г/моль.
Кулонометрический анализ позволяет определять вещества, не осаждающиеся на электродах или улетучивающиеся в атмосферу при электрохимической реакции.
Различают кулонометрию прямую и кулонометрическое титрование . Высока точность и чувствительность методов измерения электрического тока обеспечивает кулонометрическому анализу уникальную точность 0,1-0,001%, и чувствительность до 1 10 -8 ? 1 10 -10 г. Поэтому кулонометрический анализ применяется для определения микропримесей и продуктов разрушения веществ, что важно при контроле их качества.
Для индикации т.э. при кулонометрическом титровании можно применять химический и инструментальные методы - добавление индикаторов, обнаружение окрашенных соединений фотометрическим или спектрофотометрическим путём.
В отличии от других методов анализа кулонометрия может быть полностью автоматизирована, что сводит к минимуму случайные ошибки определения. Эта особенность использована при создании автоматических кулонометрических титраторов - чувствительных приборов, применяющихся для особо точных анализов, когда другие методы оказываются недостаточно чувствительными. При анализе веществ, малорастворимых в воде, кулонометрию можно проводить на электродах из ацетиленовой сажи, являющиеся хорошим адсорбентом и извлекающий такие вещества из реакционной среды с достаточной полнотой. Кулонометрическое титрование - перспективный метод инструментального анализа. Он может найти широкое применение для решения ряда специальных аналитических задач - анализа примесей, малых количеств лекарственных препаратов, определение в биологическом материале и окружающей среде токсических веществ, микроэлементов и других соединений .
ЗАКЛЮЧЕНИЕ
В работе выполнен обзор основных электрохимических методов исследования, подробно изложен их принцип, применение, преимущества и недостатки.
Электрохимические методы анализа -- группа методов количественного химического анализа, основанные на использовании электролиза.
Разновидностями метода являются электрогравиметрический анализ (электроанализ), внутренний электролиз, контактный обмен металлов (цементация), полярографический анализ, кулонометрия и др. В частности, электрогравиметрический анализ основан на взвешивании вещества, выделяющемся на одном из электродов. Метод позволяет не только проводить количественные определения меди, никеля, свинца и др., но и разделять смеси веществ.
Кроме того, к электрохимическим методам анализа относят методы, основанные на измерении электропроводности (кондуктометрия) или потенциала электрода (потенциометрия). Некоторые электрохимические методы применяются для нахождения конечной точки титрования (амперометрическое титрование, кондуктометрическое титрование, потенциометрическое титрование, кулонометрическое титрование).
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
1. Основы современного электрохимического анализа. Будников Г.К., Майстренко В.Н., Вяселев М.Р., М., Мир, 2003.
2. Дж. Плэмбек, под ред. С. Г. Майрановского Электрохимические методы анализа. Основы теории и применение: пер. с англ. / Видання: Мир, 1985.
3. Дамаскин Б.Б., Петрий О.А., Цирлина Г.А. Электрохимия - М.: химия, 2001. 624 с.
4. СТО 005-2015. Система менеджмента качества. Учебно-методическая деятельность. Оформление курсовых проектов (работ) и выпускных квалификационных работ технических специальностей.
Размещено на Allbest.ru
...Подобные документы
Классификация электрохимических методов анализа, сущность вольтамперометрии, кондуктометрии, потенциометрии, амперометрии, кулонометрии, их применение в охране окружающей среды. Характеристика химико-аналитического оборудования и основные фирмы-продавцы.
курсовая работа , добавлен 08.01.2010
Электрохимические методы основаны на измерении электрических параметров электрохимических явлений, возникающих в исследуемом растворе. Классификация электрохимических методов анализа. Потенциометрическое, кондуктометрическое, кулонометрическое титрование.
реферат , добавлен 07.01.2011
Классификация электрохимических методов анализа. Потенциометрическое определение концентрации вещества в растворе. Принцип кондуктометрии. Типы реакций при кондуктометрическом титровании. Количественный полярографический анализ. Прямая кулонометрия.
курсовая работа , добавлен 04.04.2013
Сущность электроаналитических методов, возможность получить экспериментальную информацию о кинетике и термодинамике химических систем. Достоинства, недостатки и пригодность вольтамперометрии, кондуктометрии, потенциометрии, амперометрии и кулонометрии.
реферат , добавлен 20.11.2009
Общая характеристика потенциометрического анализа. Индикаторные электроды (электронообменные и ионоселективные). Виды потенциометрического метода анализа. Прямая потенциометрия и потенциометрическое титрование. Измерение ЭДС электрохимических цепей.
курсовая работа , добавлен 08.06.2012
Общие понятия, условия проведения и классификация электрохимических методов анализа. Потенциометрический анализ (потенциометрия). Амперометрическое титрование (потенциометрическое поляризационное титрование). Количественный полярографический анализ.
реферат , добавлен 01.10.2012
Электрохимические методы исследования, их классификация и сущность история возникновения. Определение концентрации кислот методом кондуктометрического титрования; потенциалов электродов, ЭДС гальванического элемента, электрохимического эквивалента меди.
курсовая работа , добавлен 15.12.2014
Изучение метода потенциометрического анализа. Анализ и оценка объектов исследований. Изучение методики потенциометрического анализа в приложении к данному объекту. Определение возможности применения методов потенциометрического анализа мясных продуктов.
курсовая работа , добавлен 16.09.2017
Основные электрохимические методы анализа. Общая характеристика потенциометрического анализа. Виды потенциометрического метода анализа. Применение гальванического элемента, включающего два электрода. Порядок измерения потенциала индикаторного электрода.
курсовая работа , добавлен 11.08.2014
Классификация инструментальных методов анализа по определяемому параметру и способу измерения. Сущность потенциометрического, амперометрического, хроматографического и фотометрического титрования. Качественное и количественное определение хлорида цинка.
Курсовая работа
«ЭЛЕКТРОХИМИЧЕСКИЕ МЕТОДЫ
ИССЛЕДОВАНИЯ»
Введение
1. Теоретические основы электрохимических методов исследования
1.1 История возникновения метода
1.2 Описание электрохимических методов исследования
1.3 Потенциометрия
1.4 Кондуктометрия
1.5 Кулонометрия
1.6 Вольтамперометрия
1.7 Электрогравиметрия
2. Экспериментальная часть электрохимических методов исследования
2.1 Определение концентрации кислот методом кондуктометрического титрования
2.2 Потенциометрическое титрование
2.3 Электролиз
2.4 Определение потенциалов электродов
2.5 Определение ЭДС гальванического элемента
Заключение
Список используемой литературы
Введение
В современном мире всё сильнее наблюдается влияние научно-технического прогресса на все сферы нашей жизни. В связи с этим возникает необходимость более точных и быстрых методов анализа. Наиболее сильно удовлетворяют этим требованиям электрохимические методы исследования (ЭХМИ). Они являются основными физико-химическими методами исследования веществ.
ЭХМИ основаны на процессах, протекающих на электродах или межэлектродном пространстве. Являются одними из старейших физико-химических методов исследования (некоторые описаны в конце 19 века). Их достоинством является высокая точность и сравнительная простота. Высокая точность опpеделяется весьма точными закономеpностями используемыми в ЭМХИ, напpимеp, закон Фаpадея. Большим удобством является то, что в ЭХМИ используют электpические воздействия, и то, что pезультат этого воздействия (отклик) тоже получается в виде электрического сигнала. Это обеспечивает высокую скоpость и точность отсчета, откpывает шиpокие возможности для автоматизации. ЭХМИ отличаются хорошей чувствительностью и селективностью, в pяде случаев их можно отнести к микpоанализу, так как для анализа иногда достаточно менее 1 мл pаствоpа.
Оборудование, предназначенное для проведения электрохимических анализов, отличается относительной дешевизной, доступностью и простотой в использовании. Поэтому эти методы имеют широкое применение не только в специализированных лабораториях, но и на многих производствах.
Цель работы: изучение электрохимических методов исследования состава вещества.
Для достижения поставленной цели необходимо было решить следующие задачи:
рассмотреть электрохимические методы исследования, их классификацию и сущность;
изучить потенциометрическое и кондуктометрическое титрование, определение электродных потенциалов и электродвижущую силу (ЭДС) гальванического элемента, а также процесс электролиза на практике.
Объект исследования: применение электрохимических методов в анализе свойств и состава вещества.
Предмет исследования: механизмы электрохимических процессов, потенциометрия, кондуктометрия, кулонометрия, вольтамперометрия, электрогравиметрия.
электрохимический титрование гальванический
1.Теоретические основы электрохимических методов исследования
1 История возникновения метода
Систематические электрохимические исследования стало возможным проводить лишь после создания постоянного достаточно мощного источника электрического тока. Такой источник появился на рубеже 18-19 вв. в результате работ Л. Гальвани и А. Вольты. Занимаясь исследованием физиологических функций лягушки, Гальвани случайно создал электрохимическую цепь, состоящую из двух разных металлов и мышцы препарированной лапки лягушки. Когда к лапке, закрепленной с помощью медного держателя, прикасались железной проволочкой, также соединенной с держателем, мышца сокращалась. Аналогичные сокращения происходили и под действием электрического разряда. Гальвани объяснил данный феномен существованием «животного электричества». Иное толкование этим опытам дал Вольта, посчитавший, что электричество возникает в месте соприкосновения двух металлов, а сокращение мышцы лягушки - это результат прохождения через нее электрического тока. Ток возникал и в том случае, когда между двумя металлическими дисками, например цинковым и медным, помещали пропитанный соленой водой губчатый материал (сукно или бумагу) и замыкали цепь. Последовательно соединив 15-20 таких «элементов», Вольта в 1800 г. создал первый химический источник тока - «вольтов столб».
Влияние электричества на химические системы сразу заинтересовало многих ученых. Уже в 1800 г. У. Николсон и А. Карлейль сообщили, что вода разлагается на водород и кислород, когда через нее пропускают электрический ток с помощью платиновой и золотой проволочек, соединенных с «вольтовым столбом». Наиболее важными из ранних электрохимических исследований были работы английского химика Х.Дэви. В 1807 г. он выделил элемент калий, пропуская ток через слегка увлажненный твердый гидроксид калия. Источником напряжения служила батарея из 100 гальванических элементов. Аналогичным образом был получен металлический натрий. Позже Дэви, используя ртутный электрод, выделил с помощью электролиза магний, кальций, стронций и барий.
Ассистент Дэви М. Фарадей исследовал связь между количеством электричества (произведением силы тока на время), протекающего через границу раздела электрод/раствор, и вызванными им химическими изменениями. Был создан прибор (известный теперь как газовый кулонометр) для измерения количества электричества по объёму водорода и кислорода, выделившихся в электролитической ячейке, и было показано (1833), что количество электричества, необходимое для получения данного количества вещества, не зависит от размера электродов, расстояния между ними и числа пластин в питающей ячейку батарее. Кроме того, Фарадей обнаружил, что количество вещества, выделяющееся при электролизе, прямо пропорционально его химическому эквиваленту и количеству электричества, прошедшему через электролит. Эти два фундаментальных положения получили название законов Фарадея. Вместе со своим другом У. Уэвеллом, специалистом по классической филологии, Фарадей также разработал новую терминологию в электрохимии. Он назвал проводники, погруженные в раствор, электродами (ранее их называли полюсами); ввёл понятия «электролиз» (химические изменения, связанные с прохождением тока), «электролит» (проводящая жидкость в электрохимических ячейках), «анод» (электрод, на котором происходит реакция окисления) и «катод» (электрод, на котором происходит реакция восстановления). Носители заряда в жидкостях он назвал ионами (от греч. «странник», «скиталец»), причём ионы, движущиеся к аноду (положительному электроду), получили название «анионов», а к катоду - «катионов». Исследования Фарадея по электромагнитной индукции привели к созданию электрических генераторов, что позволило осуществлять электрохимические процессы в промышленных масштабах.
Способность растворов пропускать электрический ток Фарадей объяснял присутствием в них ионов, однако и он сам, и другие ученые, такие, как И. Гитторф и Ф. Кольрауш, считали, что ионы появляются под действием тока. В 1884 С.Аррениус высказал предположение, что на самом деле ионы образуются просто при растворении соли в воде. Работы С. Аррениуса, Я. Вант-Гоффа и В. Оствальда явились важной вехой в развитии теории электролитов и представлений о физико-химических свойствах растворов и их термодинамике. Соответствие теории и экспериментальных данных по ионной проводимости и равновесиям в растворе стало более полным после того, как в 1923 П. Дебай и Э. Хюккель учли дальние электростатические взаимодействия между ионами.
Первая попытка выяснить причины возникновения разности потенциалов между раствором и металлом была сделана в 1879 г. Г. Гельмгольцем, который показал, что эта разность потенциалов вызвана двойным электрическим слоем, положительная сторона которого находится на металле, отрицательная - в жидкости. Двойной слой Г. Гельмгольц рассматривал, таким образом, как плоский конденсатор. Эта модель двойного слоя долгое время оставалась вне поля зрения электрохимиков. Микромир на границе металл - раствор, где происходят электрохимические процессы, еще «ждал» своего времени.
Французский физик Ж. Гуи в 1910 г. и английский электрохимик Д. Чепмен в 1913 г. показали, что ионы электролита не располагаются в одной плоскости (как представлял Г. Гельмгольц), а образуют некоторую «диффузную» область (по мере удаления от поверхности металла концентрация ионов постепенно изменяется). Теория строения двойного слоя Гуи - Чепмена была далее развита немецким ученым О. Штерном. В 1924 г. он предложил учитывать размеры ионов и влияние адсорбции ионов и дипольных молекул растворителя при описании строения двойного электрического слоя. Изучение дифференциальной емкости двойного слоя с помощью новых методов исследования позволило советскому ученому, академику А.Н. Фрумкину в 1934-1935 гг. и американскому ученому Д. Грэму в 1941 г. установить границы применимости теории Гуи-Чепмена-Штерна. А.Н. Фрумкин предположил, что расхождение между теорией и экспериментальными данными связано с дискретным характером распределения зарядов в двойном слое. Эта идея, впервые высказанная в 1935 г., в 40-50-х годах получила дальнейшее развитие.
Серьезный вклад в электрохимическую термодинамику и конкретно в выяснение природы электрического потенциала (напряжения) в электрохимической ячейке и баланса между электрической, химической и тепловой энергией внесли Дж. Гиббс и В. Нернст. Моделированием кинетических процессов на электродах занимались Ю. Тафель (1905), Дж. Батлер (1924), М. Фольмер (1930), А.Н. Фрумкин (1930-1933).
2 Описание электрохимических методов исследования
Инстpументом для ЭХМИ служит электpохимическая ячейка, пpедставляющая собой сосуд с pаствоpом электpолита, в котоpый погpужены как минимум два электpода. В зависимости от решаемой задачи pазличными могут быть фоpма и матеpиал сосуда, число и пpиpода электpодов, pаствоpа, условия анализа (пpилагаемое напpяжение (ток) и регистрируемый аналитический сигнал, температура, перемешивание, продувка инертным газом и т.п.). Опpеделяемое вещество может входить как в состав электpолита, заполняющего ячейку, так и в состав одного из электpодов. Если окислительно-восстановительная реакция протекает на электродах ячейки самопроизвольно, то есть без приложения напряжения от внешнего источника, а только за счет разности потенциалов (ЭДС) её электродов, то такую ячейку называют гальваническим элементом. При необходимости ячейку можно подсоединить к внешнему источнику напряжения. В этом случае, приложив достаточное напряжение, можно изменить направление окислительно-восстановительной реакции и тока на противоположное тому, что имеет место в гальваническом элементе. Окислительно-восстановительную реакцию, протекающую на электродах под действием внешнего источника напряжения, называют электролизом, а электрохимическую ячейку, являющуюся потребителем энергии, необходимой для протекания в ней химической реакции, называют электролитической ячейкой.
ЭХМИ подразделяют на:
) кондуктометрию - измерение электропроводности исследуемого раствора;
) потенциометрию - измерение бестокового равновесного потенциала индикаторного электрода, для которого исследуемое вещество является потенциоопределяющим;
) кулонометрию - измерение количества электричества, необходимого для полного превращения (окисления или восстановления) исследуемого вещества;
) вольтамперометрию - измерение стационарных или нестационарных поляризационных характеристик электродов в реакциях с участием исследуемого вещества;
) электрогравиметрию - измерение массы вещества, выделенного из раствора при электролизе.
ЭХМИ можно подразделить по признаку применения электролиза. На принципах электролиза базируются кулонометрия, вольтамперометрия и электрогравиметрия; электролиз не используют в кондуктометрии и потенциометрии.
ЭХМИ имеют самостоятельное значение для прямого проведения химического анализа, но могут применяться как вспомогательные в других методах анализа. Например, использоваться в титриметрии для регистрации конца титрования не с помощью химического цветопеременного индикатора, а по изменению потенциала, электрической проводимости тока и т.д.
Рассмотрим подробнее процессы, происходящие при электрохимических исследованиях.
Электрод представляет собой систему, в простейшем случае состоящую из двух фаз, из которых твердая обладает электронной, а другая - жидкая - ионной проводимостью. Твердая фаза с электронной проводимостью считается проводником I рода, а жидкая фаза с ионной проводимостью - II рода. При соприкосновении этих двух проводников происходит образование двойного электрического слоя (ДЭС). Он может быть результатом обмена ионами между твердой и жидкой фазами, или результатом специфической адсорбции катионов или анионов на поверхности твердой фазы при погружении ее в воду или раствор.
При ионном механизме образования ДЭС, например в случае когда химический потенциал атомов на поверхности металла (твердой фазы) больше химического потенциала ионов в растворе, то атомы с поверхности металла будут переходить в раствор в виде катионов: Me ? Mez+ + ze-. Освободившиеся электроны при этом заряжают поверхность твердой фазы отрицательно и за счет этого притягивают к поверхности положительно заряженные ионы раствора. В результате на границе раздела фаз образуются два противоположно заряженных слоя, являющихся как бы обкладками своеобразного конденсатора. Для дальнейшего перехода заряженных частиц из одной фазы в другую им необходимо совершить работу, равную разности потенциалов обкладок этого конденсатора. В случае, если химический потенциал атомов на поверхности твердой фазы меньше химического потенциала ионов в растворе, то катионы из раствора переходят на поверхность твердой фазы, заряжая ее положительно: Mez+ + ze- ? Me. Как в первом, так и во втором случае указанные процессы протекают не бесконечно, а до установления динамического равновесия, которое можно изобразить обратимым редоксипереходом типа Мe - ze- ? Мez+ или в общем случае Ох + I0 ? Redz+.
Процессы, при которых отдача или присоединение электронов происходит на электродах, называются электродными.
Нернстом была получена формула, связывающая разность внутренних потенциалов ДЭС с активностями (концентрациями) частиц, участвующих в обратимом редоксипереходе:
где ? (Me) - потенциал заряженного слоя твердой фазы;
? (раствор) - потенциал прилегающего к твердой фазе слоя раствора;
??0 - стандартный электродный потенциал; - универсальная газовая постоянная (8,31 Дж/К моль); - температура, К; - число Фарадея (96 488 Кл/моль); - число электронов, участвующих в редоксипереходе;
a (Ох) и a (Red) - активности окисленной (Ох) и восстановленной (Red) форм вещества в редоксипереходе, моль/л.
Установить внутренние потенциалы отдельных фаз ? (Me) и ? (р - р), к сожалению, экспериментально нельзя. Любая попытка подключить раствор с помощью провода к измерительному устройству, вызывает появление новой поверхности соприкосновения фаз металл-раствор, то есть возникновение нового электрода со своей разностью потенциалов, влияющей на измеряемую.
Однако можно измерить разность ? (Me) - ? (р - р) с помощью гальванического элемента. Гальваническим элементом называется система, составленная из двух разных электродов, обладающая способностью самопроизвольно преобразовывать химическую энергию протекающей в нем окислительно-восстановительной реакции в электрическую энергию. Электроды, из которых составлен гальванический элемент, называются полуэлементами. Протекающая в гальваническом элементе окислительно-восстановительная реакция пространственно разделена. Полуреакция окисления протекает на полуэлементе, называемом анодом (отрицательно заряженном электроде), а полуреакция восстановления - на катоде.
Электродвижущая сила (ЭДС) гальванического элемента алгебраически складывается из разностей внутренних потенциалов составляющих его электродов. Поэтому, если в качестве одного полуэлемента взять электрод с известной величиной разности внутренних потенциалов ? (Me) - ? (раствор), то по измеренной величине ЭДС можно вычислить искомую разность потенциалов исследуемого электрода.
Для этой цели принято использовать стандартный (нормальный) водородный электрод (см. рис. 1). Он состоит из платиновой пластинки или проволоки, покрытой платиновой чернью (мелкодисперсной платиной), погруженной в раствор кислоты C=1моль/л, давление водорода над которым 0,1 МПа (1 атм). Под каталитическим влиянием платиновой черни в электроде осуществляется обратимый редоксипереход. Разность внутренних потенциалов для водородного электрода в соответствии с формулой Нернста равна:
Рисунок 1. Схема стандартного водородного электрода
так как = 1моль/л, а р (H2) = 1 атм, то
?(Me) - ?(р - р) = ??0(2H+/H2).
Решением международного союза теоретической и прикладной химии (IUPAC) условно принято считать величину ??0(2H+/H2) = 0,00 В. Очевидно, что в этом случае измеренная величина ЭДС гальванического элемента, в состав которого входит водородный электрод, равна разности внутренних потенциалов второго электрода. Эту ЭДС принято называть электродным потенциалом или редоксипотенциалом и обозначать буквой Е. Переход от внутренних потенциалов к редоксипотенциалам не меняет характера формулы Нернста:
Для большинства электродов величина электродного потенциала при единичных активностях окисленной и восстановленной форм (Е0) измерена и приведена в справочниках.
При нормальных условиях и переходе от натуральных к десятичным логарифмам предлогарифмический множитель становится равным 0,0591, и формула приобретает вид
Следует помнить, что формула Нернста связывает равновесный потенциал с активностями (концентрациями) редоксипары, т.е. потенциал, который приобретает изолированный электрод. Поэтому для аналитических цепей измерение потенциала электрода должно проводиться в условиях, максимально приближенных к равновесным: при отсутствии тока во внешней цепи гальванического элемента и через время, достаточное для достижения равновесия. Однако в реальных условиях ток может протекать через электроды. Например, ток протекает через электроды в гальваническом элементе, работа которого связана с переходом заряженных частиц через границу раздела «раствор-твердая фаза», а это направленное движение частиц есть ток. Ток протекает через электроды при электролизе, под которым подразумевают совокупность окислительно-восстановительных процессов, протекающих на электродах в растворах и расплавах электродах электролитов под действием внешнего электрического тока. При электролизе можно осуществить процессы, противоположные протекающим в гальваническом элементе.
При протекании тока (i) через электрод потенциал его изменяется и приобретает некую величину Еi, отличную от потенциала электрода в равновесных (изолированных) условиях Ер. Процесс смещения потенциала от Ер до Еi и разность Еi-Ep называют поляризацией
E=Ei-Ep. (5)
Процессам поляризации подвержены не все электроды. Электроды, потенциал которых не изменяется при протекании через них тока, называют не поляризуемыми, а электроды, для которых свойственна поляризация, называют поляризуемыми.
К не поляризуемым относятся, например, электроды II рода, к поляризуемым - все металлические и амальгамные.
1.3 Потенциометрия
Потенциометрия - электрохимический метод исследования и анализа веществ, основанный на зависимости равновесного электродного потенциала от активности концентраций определяемого иона, описываемая уравнением Нернста (1).
Зависимость электродных потенциалов от характера электродных процессов и активностей участвующих в них веществ позволяет использовать измерение ЭДС (потенциометрический метод) для нахождения коэффициентов активности электролитов, стандартных электродных потенциалов, констант равновесия, произведений растворимости, рН растворов и т. д. Преимуществами потенциометрического метода являются точность, объективность и быстрота.
Известно, что
является важной характеристикой раствора и определяет возможность и характер многих реакций.
Потенциометрическое определение рН основано на применении так называемых индикаторных электродов, в электродной реакции которых участвуют ионы водорода, а потенциал зависит от рН. Измеряя ЭДС элемента, содержащего индикаторный электрод с исследуемым раствором, можно рассчитать рН этого раствора. В качестве второго электрода должен быть взят электрод с известным потенциалом.
ЭДС элемента
H2 | исследуемый pacтвоp || KCl, Hg2Cl2 | Hg
Потенциометрический метод определения pH позволяет находить pH мутных и окрашенных сред. При использовании водородного электрода в качестве индикаторного можно определять pH растворов в широком интервале (от pH 1 до pH 14). Недостатком является необходимость длительного насыщения электрода водородом для достижения равновесия. Его нельзя применять в присутствии поверхностно-активных веществ и некоторых солей.
Схема элемента, используемого в данном случае, следующая:
| Hg2Cl2, KCl || исследуемый раствор + хингидрон | Рt,
его ЭДС равна
(10)
Потенциометрический метод определения pH раствора с использованием хингидронного электрода отличается большой простотой. Он применим для растворов с pH от 1 до 8. В щелочных средах, а также в присутствии окислителей или восстановителей хингидронный электрод непригоден.
В качестве индикаторного электрода часто используется так называемый стеклянный электрод. Он представляет собой тонкостенный стеклянный шарик, внутри которого помещен электрод сравнения, например хлорсеребряный. Стекло является переохлажденным раствором силикатов, содержащим катионы щелочных металлов и анионы типа. Стеклянный шарик предварительно выдерживается в крепком растворе кислоты, где происходит обмен катионами между стеклом и раствором и стекло насыщается ионами водорода. При определении pH в исследуемый раствор опускается стеклянный электрод и еще один электрод сравнения. В результате образуется следующая цепь:
Скачок потенциала?1 на границе стекла и раствора хлорида калия, входящего в сравнительный электрод, постоянен вследствие постоянства концентрации этого раствора. Скачок потенциала?2 зависит от концентрации исследуемого раствора и может быть записан
(11)
Где ?o и m - постоянные для данного стеклянного электрода. Учитывая скачки потенциалов на поверхности стекла, получаем
(12)
(13)
где . Отсюда
(14)
Постоянные для данного стеклянного электрода ?° и m определяют предварительной градуировкой. Для этого помещают стеклянный электрод в несколько буферных растворов с известным pH и измеряют ЭДС цепи. В дальнейшем по формуле (14) находят pH исследуемых растворов.
Перейдём к рассмотрению коэффициента активности электролита. Рассмотрим двойную концентрационную цепь без переноса, содержащую два раствора электролита:
Pt, H2 | HCl, AgCl | Ag | AgCl, HCl | H2, Pt
a 1 a 2
где a 1 и a 2 - средние ионные активности растворов HCl. Её можно использовать для определения коэффициента активности HCl. ЭДС этой цепи равна
(15)
Подстановка числовых значений R, F и Т = 298 К и переход к десятичным логарифмам даёт
(16)
Подставим в полученное уравнение
(17)
где m1 - средняя моляльность; ?1 - средний коэффициент активности электролита.
Перенесем в левую часть уравнения величины, определяемые опытным путем, и получим
(18)
Ввиду того что в предельном случае бесконечно разбавленного раствора он должен быть близок к идеальному, а ?1 ? 1, то В равна
(19)
Строим график зависимости (или, что более удобно, так как дает линию, близкую к прямой) и экстраполируем к. Таким образом определяем В графическим путем (рис. 2).
Рисунок 2. Определение коэффициента активности электролита
Коэффициент активности подсчитываем по уравнению
(20)
4 Кондуктометрия
Кондуктометрия - совокупность электрохимических методов анализа, основанных на измерении электропроводности жидких электролитов, которая пропорциональна их концентрации.
Измерения электрической проводимости (кондуктометрия) позволяют решать ряд теоретических и практических задач. Такие измерения могут осуществляться быстро и точно. При помощи кондуктометрии можно определить константу и степень диссоциации слабого электролита, растворимость и произведение растворимости труднорастворимых веществ, ионное произведение воды и другие физико-химические величины. На производстве кондуктометрические измерения используются для выбора растворов электролитов с достаточно высокой проводимостью, исключающей непроизводительные затраты электроэнергии, для быстрого и точного определения содержания растворенного вещества, для автоматического контроля за качеством различных жидкостей и т. п.
При кондуктометрическом титровании за ходом реакции следят по изменению электрической проводимости после каждого добавления титрующего реагента. Оно не требует применения индикаторов и может быть проведено в непрозрачных средах. В процессе кондуктометрического титрования происходит замена ионов титруемого вещества ионами добавляемого реагента. Точка эквивалентности определяется по резкому изменению электрической проводимости раствора, которое объясняется различной подвижностью указанных ионов.
На рис. 3 приведены кривые зависимости удельной электрической проводимости (х) от объема V приливаемого реагента. При титровании сильной кислоты сильным основанием или сильного основания сильной кислотой (кривая l) на кривой титрования образуется минимум, соответствующий замене ионов водорода или гидроксила на менее подвижные ионы образующейся соли. При титровании слабой кислоты сильным основанием илислабого основания сильной кислотой (кривая 2) в точке эквивалентности изменяется крутизна кривой, что объясняется более значительной диссоциацией образующейся соли по сравнению с диссоциацией исходного вещества. В случае титрования смеси сильной (а) и слабой (b) кислот сильным основанием (кривая 3) наблюдаются две точки эквивалентности.
Рисунок 3. Кривые кондуктометрического титрования.
С помощью таблиц ионных электрических проводимостей или путем измерений ? при разных концентрациях раствора и последующей экстраполяции к нулевой концентрации можно найти ?°. Если измерить электрическую проводимость раствора заданной концентрации, то по уравнению
(22)
получаем соотношение
(23)
Рисунок 4. Ориентация полярных молекул растворителя возле ионов электролита
Из уравнений
(24) и , (25)
полагая , получаем
(26)
(27)
Остается учесть, что величина ? обусловлена лишь данным электролитом и не включает электрическую проводимость растворителя, т. е.
5 Кулонометрия
Кулонометрия - электрохимический метод исследования, основанный на измерении количества электричества (Q), прошедшего через электролизер при электрохимическом окислении или восстановлении вещества на рабочем электроде. Согласно объединённому закону Фарадея, масса электрохимически превращённого вещества (Р) в г связана с Q в Кл соотношением:
(28)
где М - молекулярная или атомная масса вещества, n - число электронов, вовлеченных в электрохимическое превращение одной молекулы (атома) вещества (М/n - электрохимический эквивалент вещества), F - постоянная Фарадея.
Кулонометрия - единственный физико-химический метод исследования, в котором не требуются стандартные образцы. Различают прямую кулонометрию и кулонометрическое титрование. В первом случае определяют электрохимически активное вещество, во втором случае - независимо от электрохимической активности определяемого вещества в испытуемый раствор вводят электрохимически активный вспомогательный реагент, продукт электрохимического превращения которого с большой скоростью и количественно химически взаимодействует с определяемым веществом. Оба варианта кулонометрии можно проводить при постоянном потенциале Е рабочего электрода (потенциостатический режим) или при постоянном токе электролиза Iэ (гальваностатический режим). Наиболее часто используются прямая кулонометрия при постоянном Е и кулонометрическое титрование при постоянном Iэ. Для кулонометрического исследования необходимо соблюдение следующих условий: электрохимическое превращение вещества должно протекать со 100%-ным выходом по току, т.е. должны отсутствовать побочные электрохимические и химические процессы; нужны надёжные способы определения количества электричества и установления момента завершения электрохимической или химической реакции. В прямой кулонометрии 100%-ный выход по току обеспечивается, если значение Е поддерживать постоянным в области предельного диффузионного тока Iпp на вольтамперограмме определяемого вещества. При этом в анализируемом растворе должны отсутствовать посторонние вещества, способные электрохимически превращаться в тех же условиях. Количество электричества определяют обычно с помощью электронных интеграторов тока. Иногда пользуются менее точными приборами - кулонометрами различного типа, а также планометрическим и расчетными методами. В последних двух случаях завершением электролиза считают момент, когда Iэ падает до значения фонового тока Iф, поэтому количествово электричества, необходимое для завершения электродной реакции, равно разности Qоб-Qф, где Qоб - общее количество электричества, Qф - кол-во электричества, измеренное в тех же условиях за то же время электролиза tэ, но в отсутствие определяемого вещества. Если электрохимическая реакция первого порядка, то
(29)
(30)
где It и Io - ток электролиза соответственно в момент времени t и при ?=0, - площадь поверхности электрода, - коэффициент диффузии электрохимически активного в-ва,
? - толщина диффузионного слоя, - объем раствора в ячейке.
Продолжительность электролиза не зависит от начальной концентрации вещества, но заметно сокращается с увеличением соотношения S/V и при интенсивном перемешивании раствора. Можно считать электролиз завершённым, когда Iэ станет равен 0,1 I0 или 0,01 I0 (в зависимости от требуемой точности анализа). В планометрическом способе для установления Q измеряют площадь под кривой I? - ?, т.к.
(31)
В расчетном способе решают последнее уравнение, подставляя в него выражение для I?. Для нахождения I0 и К" выражение для I? логарифмируют и по нескольким (5-7) точкам строят прямую lg I?-?, тангенс угла наклона которой равен К", а точка пересечения с осью ординат соответствует lg I0, т.е. для определения Q нет необходимости проводить электролиз до конца и измерять I0, значение которого плохо воспроизводится.
Установки для кулонометрического исследования состоят из потенциостата или гальваностата, регистрирующего потенциометра или интегратора тока, электролизера и индикационной системы (в случае использования физ.-хим. методов для установления конца химической реакции в кулонометрическом титровании).
Электролизеры представляют собой, как правило, стеклянные сосуды, катодные и анодные камеры в которых разделены диафрагмой (например, из пористого стекла). В качестве рабочих и вспомогательных (замыкающих цепь электролиза) электродов используют благородные металлы (Pt, Au), электроды второго рода и, реже, углеродные материалы (графит, стеклоуглерод и др.). Раствор, в который погружен рабочий электрод, перемешивают обычно магнитной мешалкой; при необходимости эксперимент проводят в атмосфере инертного газа.
Преимущества кулонометрического титрования: нет необходимости стандартизовать растворы титранта; титрант прибавляется очень малыми порциями (практически непрерывно); раствор не разбавляется; можно генерировать электрохимически неактивные титранты, например комплексон III, а также малоустойчивые сильные окислители и восстановители, в частности Mn(III), Pb(IV), Сr(II), V(II), Ti(III).
6 Вольтамперометрия
Вольтамперометрия - совокупность электрохимических методов исследования и анализа, основанных на изучении зависимости силы тока в электролитической ячейке от потенциала погруженного в анализируемый раствор индикаторного микроэлектрода, на котором реагирует исследуемое электрохимически активное (электроактивное) вещество.
В ячейку помещают помимо индикаторного вспомогательный электрод со значительно большей чувствительностью, чтобы при прохождении тока его потенциал практически не менялся (неполяризующийся электрод). Разность потенциалов индикаторного и вспомогательного электродов Е описывается уравнением
где U - поляризующее напряжение, - сопротивление раствора.
В анализируемый раствор вводят в большой концентрации индифферентный электролит (фон), чтобы, во-первых, уменьшить величину R и, во-вторых, исключить миграционный ток, вызываемый действием электрического поля на электроактивные вещества (устар. - деполяризаторы). При низких концентрациях этих веществ омическое падение напряжения IR в растворе очень мало. Для полной компенсации омического падения напряжения применяют потенциостатирование и трехэлектродные ячейки, содержащие дополнительно электрод сравнения. В этих условиях
В качестве индикаторных микроэлектродов используют стационарные и вращающиеся - из металла (ртуть, серебро, золото, платина), углеродных материалов (напр., графит), а также капающие электроды (из ртути, амальгам, галлия). Последние представляют собой капилляры, из которых по каплям вытекает жидкий металл. Вольтамперометрия с использованием капающих электродов, потенциал которых меняется медленно и линейно, называют полярографией (метод предложен Я. Гейровским в 1922 г.). Электродами сравнения служат обычно электроды второго рода, например каломельный или хлоросеребряный. Кривые зависимости I = f(E) или I = f(U) (вольтамперограммы) регистрируют специальными приборами - полярографами разных конструкций.
Рисунок 5. Вольтамперограмма, получаемая с помощью вращающегося дискового электрода
Вольтамперограммы, полученные с помощью вращающегося или капающего электрода при монотонном изменении (линейной развёртке) напряжения, имеют вид, схематически представленный на рисунке 5. Участок увеличения тока называют волной. Волны могут быть анодными, если электроактивное вещество окисляется, или катодными, если оно восстанавливается. Когда в растворе присутствуют окисленная (Ох) и восстановленная (Red) формы веществава, достаточно быстро (обратимо) реагирующие на микроэлектроде, на вольтамперограмме наблюдается непрерывная катодно-анодная волна, пересекающая ось абсцисс при потенциале, соответствующем окислит.-восстановит. потенциалу системы Ox/Red в данной среде. Если электрохимическая реакция на микроэлектроде медленная (необратимая), на вольтамперограмме наблюдаются анодная волна окисления восстановленной формы вещества и катодная волна восстановления окисленной формы (при более отрицательном потенциале). Образование площадки предельного тока на вольтамперограмме связано либо с ограниченной скоростью массопереноса электроактивного вещества к поверхности электрода путем конвективной диффузии (предельный диффузионный ток, Id), либо с ограниченной скоростью образования электроактивного вещества из определяемого компонента в растворе. Такой ток наз. предельным кинетическим, а его сила пропорциональна концентрации этого компонента.
Форма волны для обратимой электрохимической реакции описывается уравнением:
(33)
где R - газовая постоянная, Т - абсолютная температура, - потенциал полуволны, т.е. потенциал, соответствующий половине высоты волны. Значение характерно для данного электроактивного вещества и используется для его идентификации. Когда электрохимические реакции предшествует адсорбция определяемого вещества на поверхности электрода, на вольтамперограммах наблюдаются не волны, а пики, что связано с экстремальной зависимостью адсорбции от потенциала электрода. На вольтамперограммах, зарегистрированных при линейном изменении (развертке) потенциала со стационарным электродом или на одной капле капающего электрода, также наблюдаются пики, нисходящая ветвь которых определяется обеднением приэлектродного слоя раствора электроактивным веществом. Высота пика при этом пропорциональна концентрации электроактивного вещества. В полярографии предельный диффузионный ток (в мкА), усредненный по времени жизни капли, описывается уравнением Ильковича:
(34)
где n - число электронов, участвующих в электрохимической реакции, С - концентрация электроактивного вещества, D - его коэффициент диффузии, время жизни ртутной капли, m - скорость вытекания ртути.
Вольтамперометрию применяют: для количественного анализа неорганических и органических веществ в очень широком интервале содержаний - от 10-10 % до десятков %; для исследования кинетики и механизма электродных процессов, включая стадию переноса электрона, предшествующие и последующие химические реакции, адсорбцию исходных продуктов и продуктов электрохимических реакций и т. п.; для изучения строения двойного электрического слоя, равновесия комплексообразования в растворе, образования и диссоциации интерметаллических соединений в ртути и на поверхности твердых электродов; для выбора условий ампераметрического титрования и др.
7 Электрогравиметрия
Электрогравиметрия - электрохимический метод исследования, основанный на определении увеличения массы рабочего электрода вследствие выделения на нем определяемого компонента в результате электролиза. Как правило, определяемое вещество осаждают в виде металла (или оксида) на предварительно взвешенном платиновом катоде (или аноде). Момент завершения электролиза устанавливают с помощью специфической чувствительной качественной реакции на определяемый ион. Рабочий электрод промывают, высушивают и взвешивают. По разности масс электрода до и после электролиза определяют массу выделившегося металла или оксида.
Теоретический потенциал выделения металла на катоде можно рассчитать из величин стандартных электродных потенциалов Е0. Например, при определении Cu(II) в кислом растворе на платиновых катоде и аноде протекают соответствующие реакции:
В условиях электролиза потенциал катода при 25 °С описывается уравнением Нернста:
(35)
В начале электролиза, когда поверхность катода не покрыта медью, a (Cu) бесконечно малая величина; при наличии тока, достаточного для заполнения медью поверхности катода, a (Cu) приближается к единице. На практике для протекания электрохимических реакции с заметной скоростью необходимо более высокое напряжение, чем теоретически рассчитанный потенциал выделения Е. Это связано с перенапряжением кислорода на платиновом аноде и омическим падением напряжения в ячейке.
Электрогравиметрия - селективный метод: при равенстве исходных концентраций компонентов раздельное выделение на электроде возможно при разности их электродных потенциалов порядка 0,3 В (для однозарядных ионов) или 0,1 В (для двухзарядных ионов).
Электролиз можно проводить при постоянном напряжении между электродами, при постоянной силе тока или при контролируемом потенциале рабочего электрода. В случае электрогравиметрии при постоянном напряжении происходит смещение потенциала рабочего электрода в более отрицательную область за счет поляризации. Следствием этого является снижение селективности из-за протекания дополнительной реакции (выделение других металлов или газообразного Н2). Этот вариант электрогравиметрии пригоден для определения легко восстанавливающихся веществ в присутствии примесей, восстанавливающихся труднее, чем ионы Н+. В конце электролиза возможно выделение газообразного Н2. Хотя в отличие кулонометрии 100%-ный выход по току определяемого вещества не обязателен, выделение Н2 часто приводит к образованию осадков с неудовлетворительными физическими свойствами. Поэтому в анализируемый раствор рекомендуется вводить вещества, восстанавливающиеся легче ионов Н+ (гидразин, гидроксиламин) и предотвращающие таким образом выделение Н2.
Если проводить электролиз при постоянной силе тока, необходимо периодически увеличивать налагаемое на ячейку внешнее напряжение, чтобы скомпенсировать уменьшение тока, вызываемое концентрационной поляризацией. Вследствие этого анализ становится менее селективным. Иногда, однако, удаётся связывать мешающие катионы в прочные комплексные соединения, восстанавливающиеся при более отрицательном потенциале, чем определяемое вещество, или предварительно удалять мешающий ион в виде малорастворимого соединения. Метод применяют, например, для определения Cd в щелочном растворе его цианида, Со и Ni в аммиачно-сульфатном растворе, Сu в смеси серной и азотной кислот.
Электрогравиметрия известна с 1860-х гг. и применялась для определения металлов, используемых для чеканки монет, в различных сплавах и рудах. Это безэталонный метод, который можно рассматривать как простейший вариант кулонометрии. По точности и воспроизводимости результатов электрогравиметрия превосходит другие методы при определении таких металлов, как Сu, Sn, Pb, Cd, Zn. Несмотря на относительную длительность эксперимента, электрогравиметрию до сих пор применяют для анализа сплавов, металлов и растворов для электролитных ванн.
2.Экспериментальная часть электрохимических методов исследования
1 Определение концентрации кислот методом кондуктометрического титрования
Цель лабораторной работы: определение концентрации уксусной и соляной кислот методом кондуктометрического титрования.
Оборудование и реактивы: общелабораторный модуль, компьютер, бюретка, пипетки Мора на 5 и 10 мл; растворы: 0,1 н NaOH, растворы HCl и CH3COOH с неизвестной концентрацией.
Ход работы
При проведении кондуктометрического титрования проводится два опыта:
Опыт №1
Устанавливаем бюретку и стакан. В стаканчик, находящийся в датчике прибора, наливаем пипеткой Мора 10 мл раствора соляной кислоты. Уровень раствора в стакане должен быть на 3-5 мм выше верхнего электрода и датчика. Разбавляем раствор водой. Включаем магнитную мешалку. Заполняем бюретку раствором 0,1 н. NaOH. Производим измерение с помощью общелабораторного модуля подключённого к персональному компьютеру.
Химизм процесса
Обработка результатов
1)В ходе измерения компьютер производит замеры электропроводности данного раствора, которые сведены в таблицу 1.
Таблица 1. Зависимость электропроводности от объёма щёлочи, пошедшее на титрование хлороводородной кислоты.
V(NaOH), мл0246891010,51112131415L, мСм9,2929,329,2959,2899,2789,2719,269,259,2419,219,1359,2489,256
)Строим график зависимости электропроводности от объёма щёлочи, пошедшее на титрование хлороводородной кислоты (рисунок 6).
Рисунок 6. Зависимость электропроводности от объёма щёлочи, пошедшее на титрование хлороводородной кислоты.
Vэкв (NaOH) = 13 мл
4)Используя закон эквивалентов рассчитываем концентрацию хлороводородной кислоты:
отсюда (37)
Опыт №2
Опыт проводим с 5 мл раствора уксусной кислоты. Дальнейшие действия те же, что и в предыдущем опыте.
Химизм процесса
Обработка результатов
1)В ходе измерения компьютер производит замеры электропроводности данного раствора, которые сведены в таблицу 2.
Таблица 2. Зависимость электропроводности от объёма щёлочи, пошедшее на титрование уксусной кислоты.
V(NaOH), мл012344,555,5678910L, мСм6,63,84,65,76,67,08,08,38,58,99,09,19,2
)Строим график зависимости электропроводности от объёма щёлочи, пошедшее на титрование уксусной кислоты (рисунок 7).
Рисунок 7. Зависимость электропроводности от объёма щёлочи, пошедшее на титрование уксусной кислоты.
3)По графику находим точку эквивалентности:
Vэкв (NaOH) = 5 мл
)Используя закон эквивалентов рассчитываем концентрацию уксусной кислоты:
Вывод
В ходе данной работы мы определили методом кондуктометрического титрования концентрации хлороводородной и уксусной кислот:
2 Потенциометрическое титрование
Цель : познакомиться с методом потенциометрического титрования. Установить точки эквивалентности при титровании сильной кислоты сильным основанием, слабой кислоты сильным основанием.
Оборудование : рН-метр, стеклянный электрод, хлорсеребряный электрод, стакан на 100 мл; 0,1 н. раствор НС1; СН3СООН; 0,5 н. раствор КОН; бюретка, магнитная мешалка.
Ход работы
Опыт №1
В стакан при помощи пипетки наливаем 15 мл раствора 0,1 н. соляной кислоты, опускаем бегунок, устанавливаем стакан на магнитную мешалку и включаем её после опускания электродов (следить, чтобы стеклянный электрод не касался бегунка).
Отключённое положение рН-метра «-1-14» и «0-t» нажаты. Для изменения нажимаем кнопку «рН» и снимаем значение но нижней шкале. Затем приливаем раствор 0,1 н. щелочи по 1-3 мл и фиксируем величину рН. Устанавливаем микробюретки так, чтобы щёлочь вытекала каплями. При приближении к точке эквивалентности приливаем щёлочь очень малыми дозами. Стакан во время опыта находится на магнитной мешалке, и раствор постоянно перемешиваем.
После резкого изменения рН раствора прибавляем небольшое количество щелочи и постоянно фиксируем рН.
Химизм процесса
Обработка результатов
1)В результате проведения данного опыта мы получили следующие результаты:
Таблица 3. Зависимость водородного показателя от объёма щёлочи, пошедшее на титрование уксусной кислоты.
V(KOH), мл12345678910pH4,004,154,154,004,204,304,294,945,004,91
Продолжение табл. 3
V(KOH), мл1112131415161718192021pH5,075,105,125,205,355,407,307,608,048,409,00
)По полученным данным строим график зависимости pH от объёма щёлочи, пошедшего на титрование (рисунок 8).
Рисунок 8. Кривая титрования соляной кислоты
)По графику (рисунок 8) определяем точку эквивалентности.
Vэкв (NaOH) = 16.5 мл
Опыт №2
Проводим аналогичное титрование с 0,1 н. СН3СООН.
Химизм
Обработка результатов
1)В результате проведения данного опыта мы получили следующие данные:
Таблица 4. Зависимость водородного показателя от объёма щёлочи, пошедшее на титрование уксусной кислоты.
V(KOH), мл123456789101112131415pH4,465,345,375,485,635,705,735,876,006,106,236,406,606,409,60
)По полученным данным строим график зависимости pH от объёма щёлочи, пошедшего на титрование (рисунок 9).
Рисунок 9. Кривая титрования уксусной кислоты
)По графику (рисунок 9) определяем точку эквивалентности.экв (NaOH) = 14.2 мл
Вывод
В ходе данной работы мы определили точку эквивалентности растворов хлороводородной и уксусной кислот методом потенциометрического титрования.
Точка эквивалентности для раствора хлороводородной кислоты:
Vэкв (NaOH) = 16.5 мл
Точка эквивалентности для раствора уксусной кислоты:экв (NaOH) = 14.2 мл
3 Электролиз
Цель работы : определение электрохимического эквивалента меди.
Оборудование : выпрямитель, амперметр, ванна с электролитом и двумя медными электродами, секундомер, аналитические весы, 5% раствор CuSO4, провода для монтажа прибора.
Ход работы
Электрохимический эквивалент - количество вещества, претерпевшего химическое превращение на электроде при пропускании единицы количества электричества при условии, что все пропущенное электричество тратится только на превращение данного вещества.
(38)
где Э - электрохимический эквивалент,
? - молярная масса соединения,
?q - число электронов, которое необходимо для электрохимического превращения одной молекулы этого соединения.
Молярная масса эквивалента вещества, претерпевшего химическое превращение на электроде (Мэкв) равна:
(39)
гдеm - масса отложившегося вещества,
F - постоянная Фарадея,
I - сила тока,
t - время, в течении которого протекал ток.
Для определения электрохимического эквивалента Э собираем прибор, где ток от источника пропускаем через выпрямитель и ванну с электролитом, амперметр, соединённые последовательно. При включении на медном электроде, являющийся катодом, выделяется медь. Анод, также изготовленный из меди, растворяется. Для того, чтобы медь осаждалась на катоде, образовала плотный слой и не отшелушивалась в ходе опыта, искажая результаты, следует пользоваться током, не превышающим 0,05 А на 1 см2 поверхности катода. Для этого до начала опыта при помощи миллиметровой линейки определяют поверхность катода и вычисляют максимально допустимую силу тока.
Перед началом опыта катод на 1-2 секунд погружаем в 20-30% раствор азотной кислоты, а затем тщательно промываем дистиллированной водой.
Во время проведения работы важно не дотрагиваться до поверхности катода, погруженного в электролит, т.к. даже ничтожные следы жира ухудшают адгезию катодного осадка меди.
После этого катод закрепляем в вольтметре, который наполняем раствором CuSO4. Катод вынимаем из ванны с электролитом, промываем дистиллированной водой, просушиваем и взвешиваем на аналитических весах. После этого катод вновь устанавливаем в ванну с электролитом и приступаем к опыту. Одновременно включаем ток и пускаем в ход секундомер. Опыт продолжают 40-50 минут. Одновременно выключаем ток и останавливаем секундомер. Катод вынимаем из электролита, промываем дистиллированной водой, сушим и взвешиваем.
В ходе электролиза происходили следующие химические реакции:
)Диссоциация раствора сульфата меди (II):
2)Окислительно-восстановительные реакции на электродах:
Обработка результатов
1)В результате проведения данной лабораторной работы мы получили следующие данные (таблица 5):
Таблица 5. Данные по проведённой лабораторной работе.
Сила тока (I), А1.8Время, в течении которого протекал ток (t), с2527Вес катода до опыта, выраженный в массе, г24.42Вес катода после опыта, выраженный в массе, г25.81Вес отложившегося вещества, выраженный в массе (m), г1.392)Расчёт электрохимического эквивалента:
)Расчёт молярной массы эквивалента, абсолютной и относительной ошибки:
Вывод.
В ходе данной работы мы определили электрохимический эквивалент меди, молярную массу эквивалента меди, а также абсолютную и относительную ошибку.
2.4 Определение потенциалов электродов
Цель работы : измерить потенциал медного и цинкового электродов в растворах их солей различной активности. Сравнить измеренные значения потенциалов с расчётами по уравнению Нернста.
Оборудование : pH-метр, медный электрод, цинковый электрод, хлорсеребряный электрод, U-образная трубка с насыщенным раствором KCl, наждачная бумага, растворы CuSO4 и ZnSO4 с различной концентрацией.
Ход работы
Для измерения потенциалов 1 рода собираем цепь, состоящую из измерительного прибора, измеряемого электрода и электрода сравнения. Фактически мы измеряем ЭДС гальванического элемента
| AgCl, KCl || CuSO4 | Cu;
Zn | ZnSO4 || KCI, AgCl | Ag.
Потенциал хлорсеребряного электрода (электрод 2 рода) постоянен, зависит только от активности ионов Cl и равен Ag | AgCl (насыщенный раствор КС1) = 0,2 В. Он является электродом сравнения.
Для устранения диффузного потенциала используем мостики, заполненные насыщенным раствором KCl.
Для измерения потенциалов используем рН-метр. Хлорсеребряный электрод подсоединяем к специальному гнезду «электрод сравнения» (на ВСП панели прибора), а измерительный электрод через специальный штекер к гнезду «изм - 1», «изм - 2».
Химизм процессов
Для гальванического элемента Ag | AgCl, KCl || CuSO4 | Cu:
Для гальванического элемента Zn | ZnSO4 || KCI, AgCl | Ag:
Обработка результатов
1)В результате измерения потенциалов медного электрода при различной активности ионов Cu2+ мы получили следующие данные:
¾для медного электрода (таблица 6):
Таблица 6. Данные по проведённой лабораторной работе для медного электрода.
?изм, ВCн, моль * экв-1 * л-1?lg a?вычисл, В0,2100,10,38-1,72120,2862230,3510,20,36-1,44370,2944110,3600,50,25-1,20410,3014780,3611,00,23-0,93930,309291
¾для цинкового электрода (таблица 7):
Таблица 6. Данные по проведённой лабораторной работе для цинкового электрода.
?изм, ВCн, моль * экв-1 * л-1?lg a?вычисл, В-0,0650,10,25-1,9031-0,81914-0,0650,20,28-1,5528-0,80881-0,0290,50,38-1,0223-0,79316-0,0501,00,40-0,6990-0,78362
2)Строим график зависимости потенциала электрода от lg а(Cu2+).
¾для медного электрода (рисунок 10):
Рисунок 10. Зависимость потенциала электрода от логарифма активности ионов меди (II)
¾для цинкового электрода (рисунок 11):
Рисунок 11. Зависимость потенциала электрода от логарифма активности ионов цинка
.Вычисляем потенциалы электродов по уравнению Нернста (1):
¾для медного электрода:
¾для цинкового электрода:
Вывод : в ходе данной работы мы измерили потенциалы медного и цинкового электродов при различных концентрациях CuSO4 и ZnSO4 соответственно, а также рассчитали эти электродные потенциалы по уравнению Нернста, в следствие чего сделали вывод, что с увеличением концентрации электродные потенциалы у медного и цинкового электрода возрастают.
5 Определение ЭДС гальванического элемента
Цель: определить ЭДС гальванического элемента.
Оборудование : цинковый и медный электрод, растворы CuSO4 и ZnSO4, хлорсеребряный электрод, рН-метр, наждачная бумага, U-образная трубка с насыщенным раствором КС1, 0,1н. и 1н. раствор CuSO4, 0,1н. и 1н. раствор ZnSO4,
Ход работы
В два стакана наливаем наполовину растворы CuSO4 и ZnSO4. В первый помещаем электрод из меди, во второй - из цинка.
Электроды предварительно зачищаем наждачной бумагой и промываем. Провода подсоединяем к рН-метру на задней панели к входам «Изм.1» и «Эл. сравн». Внешнюю цепь замыкаем при помощи U-образной трубки, заполненной насыщенным раствором KCl в агар-агаре.
Перед измерением прибор прогревается в течении 30 минут. Когда собрана цепь приступаем к измерениям, нажимаем кнопку «mV» и смотрим показания прибора по нижней шкале «1-14». Для более точного определения ЭДС нажимаем кнопку нужного диапазона. Для перевода измеренных значений в вольты числитель значения умножаем на 0,1.
Для выполнения работы измеряем ЭДС элементов в растворах с концентрацией 1н. и 0,1н. и сравниваем эти данные с расчетами. Находим абсолютную и относительную ошибку.
Химизм процессов
Для данного гальванического элемента
| ZnSO4 || KCI, AgCl | Ag
характерны следующие реакции:
Суммарное уравнение реакции протекающей в медно-цинковом гальваническом элементе:
Обработка результатов
1)В результате проведения данной работы мы получили следующие результаты (таблица 6):
Таблица 6. Данные по проведённой лабораторной работе
Растворы?изм, В?вычисл, ВОтносительная ошибка, %0,1н. CuSO4 и 0,1н. ZnSO41,0871,0991,0921н. CuSO4 и 0,1н. ZnSO41,0821,0931,0061н. CuSO4 и 1н. ZnSO41,0601,070,935
)Проводим расчёт ЭДС:
Расчёт потенциалов проводим по уравнению Нернста (1). Стандартные электродные потенциалы взяты из справочных данных.
Для растворов 0,1н. CuSO4 и 0,1н. ZnSO4:
Для растворов 1н. CuSO4 и 0,1н. ZnSO4:
Для растворов 1н. CuSO4 и 1н. ZnSO4:
Вывод : в данной работе мы определили ЭДС гальванического элемента в растворах различной концентрации:
при концентрации 0,1н. CuSO4 и 0,1н. ZnSO4,
при концентрации 1н. CuSO4 и 0,1н. ZnSO4,
при концентрации 1н. CuSO4 и 1н. ZnSO4;
а также определили относительную ошибку: 1,092%, 1,006%, 0,935% соответственно. В следствии чего сделали вывод, что при увеличении концентрации растворов Э.Д.С. у гальванического элемента уменьшается.
Заключение
В данной работе мы рассмотрели основные методы электрохимических исследований, разобрали их классификацию, основные электрохимические процессы, а также доказали актуальность данных методов. Большая часть работы была отведена на описание электродных процессов. Подробно были изучены потенциометрия, кондуктометрия, кулонометрия, вольтамперометрия и электрогравиметрия.
В ходе практических исследований мы провели: определение концентрации неизвестных кислот методом кондуктометрического титрования, определение точки эквивалентности растворов хлороводородной и уксусной кислот методом потенциометрического титрования, определение электрохимического эквивалента меди, определение потенциалов медного и цинкового электродов, и определение ЭДС гальванического элемента.
Мы убедились быстроте и точности данных методов, но в тоже время на собственном опыте выявили некоторые существенные недостатки: для получения точных данных необходима очень точная настройка и калибровка приборов, полученные результаты зависят от различных внешних факторов (давление, температура и др.) и при других условиях могут существенно различаться, а также хрупкость и высокая стоимость приборов.
И всё же, это далеко не все известные методы электрохимических исследований. Все приведённые методы являются лишь малой частью электрохимических методов исследований используемых в науке и техники. А используются они настолько широко во всех отраслях промышленности, что без них невозможно ни существование, ни дальнейшее развитие цивилизации. Несмотря на солидный возраст, электрохимические методы исследований переживают бурное развитие с огромными перспективами на будущее. По прогнозам ряда ведущих учёных их роль будет стремительно возрастать.
Осталось лишь всячески способствовать развитию в этом направлении и возможно в будущем нам откроются такие тайны и области применения электрохимических методов исследования, о которых можно было только мечтать.
Список используемой литературы
Агасян П.К., Хамракулов T.К. Кулонометрический метод анализа. Mосква: Химия. 2010. 168 с.
Брайнина Х.З., Нейман Е.Я. Твёрдофазные реакции в электроаналитической химии. Москва: Химия. 2009. 264 с.
Галюс З. Теоретические основы электрохимического анализа: перевод с польского. Москва: Мир. 1974. 552 с.
Гейровский Я., Кута Я. Основы полярографии: перевод с чешского. Под редакцией С.Г. Майрановского. Москва: Мир. 1965. 559 с.
Голиков Г.А. Руководство по физической химии: Учебное пособие для химико-технологических специализированных вузов. Москва: Высшая школа. 2008. 383 с.
Зозуля А.Н. Кулонометрический анализ, 2 издание, Ленинград: Химия. 1968. 160 с.
Кнорре Д.Г., Л.Ф. Крылова. В.С. Музыкантов. Физическая химия: Учебное пособие для биологических факультетов университетов и педагогических вузов. 2 издание. Москва: Высшая школа. 1990. 416 с.
Левин А.И. Теоретические основы электрохимии. Москва: Металлургиздат. 1963. 432 с.
Лопарин Б.А. Теоретические основы элетрохимических методов анализа. Москва: Высшая школа. 1975. 295 с.
Плембек Д. Электрохимические методы анализа: основы теории и применение. Москва: Мир. 2009. 496 с.
Соловьёв Ю.И. История химии: Развитие химии с древнейших времён до конца XIX в. Пособие для учителей. 2 издание. Москва: Просвещение. 2007. 368 с.
Фигуровский Н.А. История химии: Учебное пособие для студентов педагогических институтов по химическим и биологическим специальностям. Москва: Просвещение. 1979. 311 с.
Физическая химия: программа дисциплины и учебно-методические рекомендации / составители А.Н. Козлов, Н.П. Ускова. Рязань: Рязанский государственный университет имени С.А.Есенина. 2010. 60 с.
Физическая химия. Теоретическое и практическое руководство. Учебное пособие для ВУЗов / Под редакцией академика Б.П. Никольского. 2 издание. Ленинград: Химия, 1987, 880 с.
Харнед Г. Оуэр Б. Физическая химия растворов электролитов. Москва: ИИН. 2011. 629 с.
Юинг Г. Инструментальные методы химического анализа. Москва: Мир. 2011. 620 с.
Книга: многотомное издание
Методы измерения в электрохимии / редакторы Э.Егер и А.Залкинд, перевод с английского кандидатами физико-математических наук В.С. Маркина и В.Ф. Пастушенко, под редакцией доктора химических наук Ю.А. Чизмаджева. Москва: Мир, 1977. Т. 1-2.
Скуг Д., Уэст Д. Основы аналитической химии. Москва: Мир, 1979. Т. 2
Эткинс П. Физическая химия. Москва: Мир, 1980. Т. 1-2.
Репетиторство
Нужна помощь по изучению какой-либы темы?
Наши специалисты проконсультируют или окажут репетиторские услуги по интересующей вас тематике.
Отправь заявку
с указанием темы прямо сейчас, чтобы узнать о возможности получения консультации.

 Всеволод большое гнездо как правитель
Всеволод большое гнездо как правитель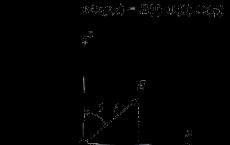 Как заполняются электронные уровни, подуровни и орбитали по мере усложнения атома
Как заполняются электронные уровни, подуровни и орбитали по мере усложнения атома Самые первые спички в мире
Самые первые спички в мире